

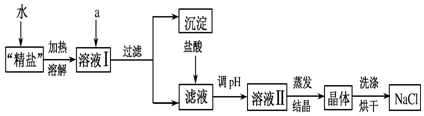
分析 (1)操作⑤由滤液得到晶体,为蒸发操作;
(2)发现制得率较低,说明实际称量得到的精盐质量偏小;
(3)粗盐中含有少量的MgCl2、CaCl2等可溶性杂质,可加入NaOH溶液、Na2CO3溶液,分别生成氢氧化镁、碳酸钙等沉淀,滤液含有氯化钠、氢氧化钠和碳酸钠,加入盐酸调节pH得到氯化钠,蒸发、结晶可得到纯净的氯化钠.
解答 解:(1)操作⑤由滤液得到晶体,为蒸发操作,需要铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳、蒸发皿等仪器,故答案为:蒸发皿;
(2)A.粗盐未能完全溶解,过滤得到的氯化钠固体偏少,会导致产率偏低,故A正确;
B.过滤或蒸发时有液体飞溅,造成了氯化钠的损耗,会导致产率偏低,故B正确;
C.蒸发时没有蒸发至干,得到的氯化钠质量偏低,会导致产率偏高,故C错误;
D.蒸发皿上粘有的“精盐”没有全部转移到称量纸上,会导致产率偏低,故D正确.
故答案为:ABD;
(3)①粗盐中含有少量的MgCl2、CaCl2等可溶性杂质,可加入NaOH溶液、Na2CO3溶液,分别生成氢氧化镁、碳酸钙等沉淀,反应的离子方程式为Mg2++2OH-=Mg(OH)2↓、CO32-+Ca2+=CaCO3↓,
故答案为:NaOH溶液、Na2CO3溶液;Mg2++2OH-=Mg(OH)2↓、CO32-+Ca2+=CaCO3↓;
②滤液含有氯化钠、氢氧化钠和碳酸钠,加入盐酸调节pH得到氯化钠,发生反应为HCl+NaOH═NaCl+H2O、2HCl+Na2CO3═2NaCl+CO2↑+H2O,
故答案为:HCl+NaOH═NaCl+H2O、2HCl+Na2CO3═2NaCl+CO2↑+H2O.
点评 本题考查粗盐的提纯,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验的操作原理、方法以及注意事项,难度不大.


科目:高中化学 来源: 题型:解答题
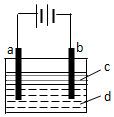 由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图所示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.
由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图所示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
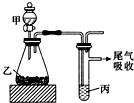
| 甲 | 乙 | 丙 | 结论 | |
| A | 水 | 电石 | 溴水 | 稳定性:H2O>C2H2>Br2 |
| B | 盐酸 | 硫化亚铁 | 溴水 | 还原性:Cl->Br->S2- |
| C | 浓盐酸 | 高锰酸钾 | 溴化钾溶液 | 氧化性:高锰酸钾>Cl2>Br2 |
| D | 盐酸 | 石灰石 | 苯酚钠溶液 | 酸性:HCl>H2CO3>苯酚 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答:
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①② | C. | ③⑤ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com