
 �±��������ֶ�����Ԫ�ص������Ϣ��
�±��������ֶ�����Ԫ�ص������Ϣ��| Ԫ�� | �����Ϣ |
| A | ���¡���ѹ�£��䵥������������壬������Ϊ�������������ȼ�� |
| B | ��ҵ��ͨ������Һ̬��������䵥�ʣ���ij��ͬ���������DZ�������ر���������Ҫ���� |
| C | ֲ��������Ҫ��֮һ�������γɶ��������ijЩ���������ɹ⻯ѧ��Ⱦ |
| D | �������䵥��Ϊ����ɫ��ĩ״���壬�������ۻ����õ�����������ȼ�գ���������������ɫ���� |
| E | �������䵥��Ϊ����ɫ���壬�䵥��ˮ��Һ��Ư�ס�ɱ������ |
 ��
������ A��B��C��DΪ������Ԫ�أ�������ȼ�ղ���Ϊˮ���DZ������������ȼ�ϣ���AΪH������Һ̬�����ɵõ������������������ܱ�������ر���������BΪO��C��ֲ���������ֱ���Ԫ��֮һ�������γɶ�������������γɶ�����������⻯������ѧ��ѧ��ѧϰ��Ψһ�ļ������壬��ʹʪ��ĺ�ɫʯ����ֽ��������CΪN��������D�ĵ��ʳʷ�ĩ״���壬�������ۻ����õ�����������ȼ�գ���������������ɫ���棬��DΪS��E�������䵥��Ϊ����ɫ���壬�䵥��ˮ��Һ��Ư�ס�ɱ�����ã���EΪCl��Ȼ������Ԫ�ؼ��䵥�ʡ�����������������
��� �⣺A��B��C��DΪ������Ԫ�أ�������ȼ�ղ���Ϊˮ���DZ������������ȼ�ϣ���AΪH������Һ̬�����ɵõ������������������ܱ�������ر���������BΪO��C��ֲ���������ֱ���Ԫ��֮һ�������γɶ�������������γɶ�����������⻯������ѧ��ѧ��ѧϰ��Ψһ�ļ������壬��ʹʪ��ĺ�ɫʯ����ֽ��������CΪN��������D�ĵ��ʳʷ�ĩ״���壬�������ۻ����õ�����������ȼ�գ���������������ɫ���棬��DΪS��E�������䵥��Ϊ����ɫ���壬�䵥��ˮ��Һ��Ư�ס�ɱ�����ã���EΪCl��
��1��DΪS����������Ų� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2��A��B��Ԫ���γɵĺ��зǼ��Լ��Ļ�����������⣬��ṹʽΪH-O-O-H���⡢����Ԫ���γɵľ�����ͬ��������������OH-��H3O+���ʴ�ΪH-O-O-H��OH-��H3O+��
��3���������γɵ�ijһ������N2H4�ܺ͵������γɵ���һ��ɫ������N2O4�����߷�����Ӧ�����������ǵ�������Ӧ����ʽΪ��2N2H4+N2O4�T3N2+4H2O���ʴ�Ϊ��2N2H4+N2O4�T3N2+4H2O��
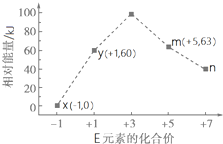
��4��n����+7�۵����ӷ���Ϊ��ClO4-�����ӷ�Ӧy��x+m��y��������������ԭ��Ӧ����x��m������ת�Ƶ����غ�ø÷�Ӧ����ʽΪ3ClO-=ClO3-+2Cl-����Ӧ��=��63kJ/mol+2��0kJ/mol��-3��60kJ/mol=-117kJ/mol���ʴ�Ϊ��ClO4-��3ClO-��aq��=2Cl-��aq��+ClO3-��aq����H=-117 kJ•mol-1��
��5��Na2SO3ˮ��Һ�ʼ��ԣ���Һ�и�����Ũ�ȵĴ�С˳����Na+��SO32-��OH-��HSO3-��H+���ʴ�Ϊ��Na+��SO32-��OH-��HSO3-��H+��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã���ϤԪ�ؼ����ʵ������ǽ����Ĺؼ����ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ���Ҵ��ͱ��Ӷ����ܵ��� | |
| B�� | �������б������ǻ��Ļ�����һ���Ƿ� | |
| C�� | ���״���2-�����ӻ�Ϊͬ���칹�� | |
| D�� | �Ӻʹ�������ͬ�Ĺ����ţ����������ͬ�Ļ�ѧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����445.2KJ | B�� | ����480.4KJ | C�� | �ų�445.2KJ | D�� | �ų�480.4KJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | 1��3-����ϩ | ||
| C�� | �ұ� | D�� | 2-��-1��3-����ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��W���������Ϊ+7��
��W���������Ϊ+7���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ķ���ʽ Cl | B�� | ��ԭ�ӵĽṹʾ��ͼ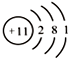 | ||
| C�� | N2�ĵ���ʽ��N������N�� | D�� | NaCl�ĵ���ʽ Na+��Cl�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
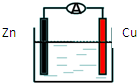
| A�� | п����������������Ӧ | |
| B�� | ����ʱ���ܷ�ӦΪ��Zn+2H+=Zn2++H2�� | |
| C�� | ��װ�ÿ�ʵ�ֻ�ѧ��ת��Ϊ���� | |
| D�� | ��Һ�������������Cu���ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �����¶ȣ�H2SŨ�����ӣ������÷�Ӧ�Ƿ��ȷ�Ӧ | |
| B�� | ͨ��CO������Ӧ���������� | |
| C�� | ��ӦǰH2S���ʵ���Ϊ7mol | |
| D�� | CO��ƽ��ת����Ϊ80% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com