
将下图所示实验装置的K闭合,下列判断正确的是 ( )
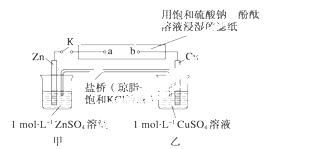
A.Cu电极上发生还原反应
B.电子沿 Zn→a→b→Cu 路径流动
C.片刻后甲池中c(SO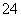 )增大
)增大
D.片刻后可观察到滤纸b点变红色
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
下列有关钢材在空气中生锈的说法正确的是( )
A.红色铁锈的主要成分是Fe(OH)3
B.钢材在空气中的反应只有氧化、还原及化合反应
C.钢材在空气中的腐蚀主要为电化学腐蚀,其负极的反应为:Fe-3e-====Fe3+
D.太阳、风雨、湿度对钢材的腐蚀有较大影响
查看答案和解析>>
科目:高中化学 来源: 题型:
实验发现,298 K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。某夏令营兴趣小组根
据该实验事实设计了如图所示原电池装置。下列有关说法正确的是 ( )
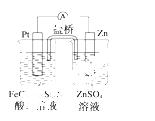 A.该原电池的正极反应是Zn-2e-===Zn2+
A.该原电池的正极反应是Zn-2e-===Zn2+
B.左烧杯中溶液的血红色逐渐褪去
C.该电池铂电极上有气泡出现
D.该电池总反应为3Zn+2Fe3+===2Fe+3Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次(从左至右)发生的反应类型和反应条件都 正
确的是 ( )
| 选项 | 反应类型 | 反应条件 |
| A | 加成反应、取代反应、消去反应 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
| B | 消去 | NaOH醇溶液/加热、常温、NaOH水溶液/加热 |
| C | 氧化反应、取代反应、消去反应 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
| D | 消去反应、加成反应、水解反应 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 控制适合的条件,将反应2Fe3++2I-
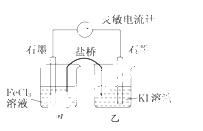
控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成
2Fe2++I2设计成 如下图所示的原电池.下列判断不正确的是 ( )
如下图所示的原电池.下列判断不正确的是 ( )
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中的石墨电极为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
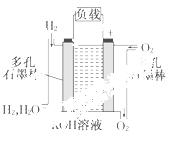 被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、
被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、
无噪音、高效率的特点.右图为氢氧燃料电池的结构示意图,电解质溶液为
KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、
负两极通入燃料电池时,便可在闭合回路中不断地产生电流。
试回答下列问题:
(1)图中通过负载的 电子流动方向________(填“向左”或“向右”).
电子流动方向________(填“向左”或“向右”).
(2)写出氢氧燃料电池工作时电极反应方程式和总反应方程式.
正极:________________________________________________________,
负极:________________________________________________________________,
总反应:__________________________________________________________.
(3 )为了获得氢气,除了充分利用太阳能外,工业上利用石油产品与水在催化剂作用下制取氢气.写出C3H8和H2O反应生成H2和CO的化学方程式:_____________________________________;
)为了获得氢气,除了充分利用太阳能外,工业上利用石油产品与水在催化剂作用下制取氢气.写出C3H8和H2O反应生成H2和CO的化学方程式:_____________________________________;
(4)若将此燃料电池改进为直接以甲烷和氧气为原料进行工作时,正极反应式为________________;
负极反应式为____________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
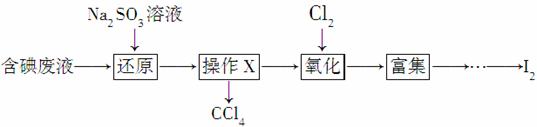
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为__________________;该操作将I2还原为I-的目的是________。
(2)操作X的名称为________。
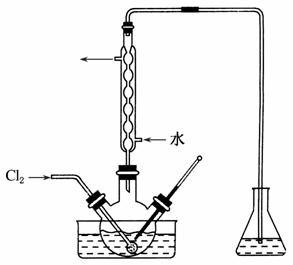
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40 ℃左右反应(实验装置如右图所示)。
实验控制在较低温度下进行的原因是__________;锥形瓶里盛放的溶液为__________。
(4)已知:5SO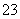 +2IO
+2IO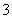 +2H+===I2+5SO
+2H+===I2+5SO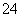 +H2O
+H2O
某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO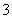 中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO
中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO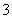 的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在________________________。
的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在________________________。
实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语或模型表示不正确的是
A.中子数为14的硅原子: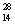 Si
Si
B.CH4分子的比例模型:
C.聚乙烯的结构简式: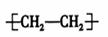
D.次氯酸分子的结构式:H—O-Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com