
| A. | 世博会期间,利用可降解的“玉米翅料”替代一次性饭盒,可防止产生白色污染 | |
| B. | 世博停车场安装催化光解设施,可将汽车尾气中CO和NOx反应生成无毒气体 | |
| C. | 利用太阳能、风能和氢能等能源替代化石能源有利于实现“低碳经济” | |
| D. | 高纯度的硅单质广泛用于制作光导纤维 |
分析 A.一次性饭盒的主要材料为聚乙烯,难降解;
B.CO和NOx之间反应生成氮气和二氧化碳无毒气体;
C.太阳能、风能和氢能等能源不产生二氧化碳;
D.硅能作硅太阳能电池板、半导体材料、硅芯片,光导纤维的主要成分是二氧化硅.
解答 解:A.普通塑料不能降解,玉米塑料具有良好的生物相容性和可降解性广泛使用可有效地解决“白色污染”,故A正确;
B.安装催化光解设施,这样汽车尾气中的CO和NOx可以转化为氮气和二氧化碳,均是无毒气体,防止污染空气,故B正确;
C.太阳能、风能和氢能等能源不产生二氧化碳,故有利于实现“低碳经济”,故C正确;
D.硅能作硅太阳能电池板、半导体材料、硅芯片,光导纤维的主要成分是二氧化硅,是利用光的全反射原理,故D正确;
故选D.
点评 本题考查环境污染、物质用途等知识点,为高频考点,明确元素化合物性质、物质用途等知识点是解本题关键,会运用化学知识解答生活问题,学以致用.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3溶液与过量NaOH溶液反应 NH4++OH-=NH3↑+H2O | |
| B. | 过量CO2通入Ca(ClO)2溶液中 ClO-+CO2+H2O=HCO3-+HClO | |
| C. | 向Na2CO3溶液中加入过量CH3COOH溶液 CO32-+2H+=CO2↑+H2O | |
| D. | 向Ba(OH)2溶液中加入少量NaHSO3溶液 2HSO3-+Ba2++2OH-=BaSO3↓+SO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 元素性质或原子结构信息 |
| Q | 原子核外有6种不同运动状态的电子 |
| R | 最外层电子数是次外层电子数的3倍 |
| X | 气态氢化物的水溶液呈弱碱性 |
| Y | 第三周期元素的简单离子中离子半径最小 |
| Z | 单质为银白色固体,在空气中燃烧发出黄色火焰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.075mol/L | B. | 0.1125mol/L | C. | 0.15mol/L | D. | 0.225mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
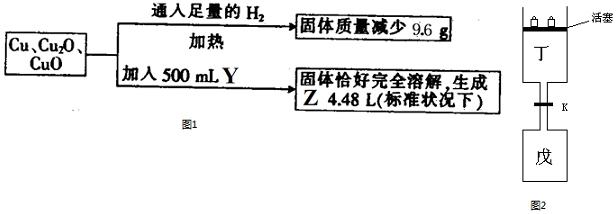
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
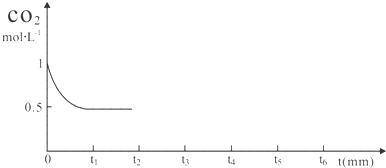
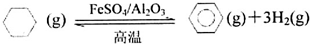
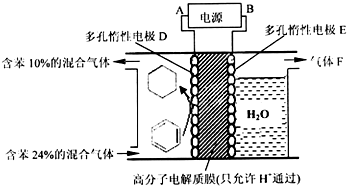
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
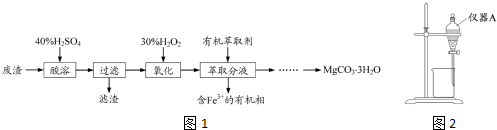
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.2mol | B. | 2mol | C. | 0.8mol | D. | 1.8mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com