
氯水中存在多种微粒,下列有关粒子的表示方法正确的是 ( )
A.氯气的电子式:Cl Cl
Cl
B.氢氧根离子的电子式: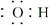
C.次氯酸分子的结构式:H—O—Cl
D.HClO的电子式: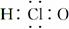
科目:高中化学 来源: 题型:
葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2
相关物质的溶解性见下表:
| 物质名 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
实验流程如下:
C6H12O6溶液


 悬浊液
悬浊液

 Ca(C6H11O7)2
Ca(C6H11O7)2
请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,下列装置最合适的是________。

制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是________。
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第② 步充分反应后CaCO3固体需有剩余,其目的是________;本实验中不宜用CaCl2替代CaCO3,理由是________。
步充分反应后CaCO3固体需有剩余,其目的是________;本实验中不宜用CaCl2替代CaCO3,理由是________。
(3)第③步需趁热过滤,其原因是________。
(4)第④步加入乙醇的作用是________。
(5)第⑥步中,下列洗涤剂最合适的是________。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
I、A、B、C、D、E都是短周期元素,原子半径D>C>A>E>B,其中A、B处在同一周期,A、C处在同一主族。C原子核内质子数等于A、B原子核内质子数之和,C原子最外层上的电子数是D原子最外层电子数的4倍,且D为金属。试回答:
(1) 在五种元素中,能形成的最简单的液态或气态氢化物的稳定性由大而小的顺序是(用具体的分子式表示)
(2) A与B形成的三原子分子的结构式是 ,B与D形成的原子个数比为1∶1的化合物的电子式是 。
(3) E的一种氢化物叫肼,其分子中E原子与氢原子个数比为1 :2。已知32克液态肼在氧气中完全燃烧生成氮气和液态水放热624KJ则该反应的热化学方程式为__________________。
(4) 肼—空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%—30%的KOH溶液。该燃料电池的正极的电极反应式是____________。
II、 现有如下两个反应:
(A)NaOH + HCl =NaCl + H2O
(B)2FeCl3 + Cu = 2FeCl2 + CuCl2
(5)根据能设计成原电池的反应选择适宜的材料和试剂设计一个原电池:
请画原电池装置示意图(注明电极正负极、电极材料、电解质溶液)
常用来冶炼该电池负极材料的两种方法是(用化学方程式表示)_________、_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
分子式为C5H10O2的有机物在酸性条件下可水解为酸和醇,若不考虑立体异构,这些醇和酸重新组合可形成的酯共有 ( )
A、15种 B、28种 C、32种 D、40种
查看答案和解析>>
科目:高中化学 来源: 题型:
 有机化合物 G
有机化合物 G  的合成线路如下:
的合成线路如下:

其中A~F分别代表一种有机化合物,合成路线中的部分产物及反应条件已略去。
已知:

请回答下列问题:
⑴G的分子式是 ;G中官能团的名称是 。
⑵第②步反应的化学方程式是 。
⑶第②~⑥步中属于取代反应的有 (填步骤编号)。
⑷第④步反应的化学方程式是 。
⑸写出同时满足下列条件的E的任意两种同分异构体的结构简式 、
。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是
( )
A.NH4Cl NH3↑+HCl↑
NH3↑+HCl↑
B.NH3+CO2+H2O===NH4HCO3
C.2NaOH+Cl2===NaCl+NaClO+H2O
D.2Na2O2+2CO2===2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是________,非金属性最强的是________(填元素符号)。
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是________(用化学式表示)。
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为________,其中存在的化学键类型为________。
(4)D最高价氧化物的水化物的化学式为________。
(6)单质E与水反应的离子方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
A.质子数:c>d B.离子的还原性:Y2->Z-
C.氢化物的稳定性:H2Y>HZ D.原子半径:X<W
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com