
| A、食盐放在水中片刻后消失了 |
| B、食醋洒在大理石台面上产生气泡 |
| C、烧菜用过的铁锅,放置后常出现红棕色斑迹 |
| D、用食醋可以除去水壶中的水垢[水垢的主要成分为CaCO3、Mg(OH)2] |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、糖类是具有甜味的物质 |
| B、糖类是具有Cn(H2O)m通式的物质 |
| C、葡萄糖是一种单糖的主要原因是一种多羟基醛 |
| D、淀粉是一种白色粉末,本身没有甜味 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将58.5g NaCl固体溶于1 L水中所得溶液 |
| B、将22.4L HCl气体溶于水配成1 L的溶液 |
| C、从1L 10mol/L的浓盐酸中取出的100mL溶液 |
| D、将4g NaOH固体溶于水中配成的100 mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化合物KCrO2中Cr元素为+3价 |
| B、实验①证明Cr2O3是两性氧化物 |
| C、实验②证明氧化性:Cr2O72-<I2 |
| D、实验③证明H2O2有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在通常条件下,1mol氩气含有的原子数为2NA |
| B、56g金属铁由原子变为离子时失去的电子数为NA |
| C、在标准状况下,2.24 L氨气所含的电子总数约为NA |
| D、1 mol/L 的 Na2SO4溶液中含有Na+个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深 |
| B、氧族元素氢化物稳定性按H2O、H2S、H2Se、H2Te的顺序依次减小 |
| C、氢化物的沸点按NH3、BiH3、SbH3、AsH3、PH3的顺序依次递减 |
| D、最高价氧化物对应水化物碱性按NaOH、KOH、RbOH、CsOH的顺序依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两者的分散质都属于碱 |
| B、两者均为有色不透明的分散系 |
| C、两者分散质的直径都介于10-9~10-7m之间 |
| D、两者都有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢钙溶液和过量氢氧化钙溶液混合:Ca2++2HCO3-+OH-═CaCO3↓+CO32-+H2O |
| B、CuCl2溶液与Na2S溶液2:1反应,Cu2++S2-═CuS↓ |
| C、用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |
| D、向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -═2 Al(OH)3↓+3BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
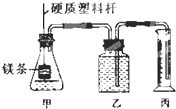 某研究性学习小组为证明在相同条件下,同浓度同体积强弱不同的一元酸与同一种金属反应时,生成氢气的速率不同,同时测定该温度和压强下的气体摩尔体积,设计组装了两套如图所示的简易实验装置.
某研究性学习小组为证明在相同条件下,同浓度同体积强弱不同的一元酸与同一种金属反应时,生成氢气的速率不同,同时测定该温度和压强下的气体摩尔体积,设计组装了两套如图所示的简易实验装置.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com