
下列离子方程式正确的
A.向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO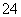 ===BaSO4↓
===BaSO4↓
B.双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-===I2+2H2O
C.用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
D.Na2S2O3溶液中加入稀硫酸:2S2O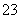 +4H+===SO
+4H+===SO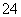 +3S↓+2H2O
+3S↓+2H2O
科目:高中化学 来源: 题型:
生活中难免会遇到一些突发事件,我们要善于利用学过的知识,采取科学、有效的方法保护自己。如果发生了氯气泄漏,以下自救方法得当的是( )
A.只要在室内放一盆水 B.向地势低的地方撤离
C.观察风向,顺风撤离 D.用湿毛巾或蘸有纯碱水的毛巾捂住口鼻撤离
查看答案和解析>>
科目:高中化学 来源: 题型:
实验是进行化学研究的重要手段之一。请回答下列问题:
(1)下列实验操作,正确的是____________________(填写序号)。
a. 称取氢氧化钠固体时,应将氢氧化钠固体直接放在左边托盘内,右边托盘放砝码
b. 用纸槽往试管里装粉末状药品时,试管应先横放再直立
c. 试管、烧杯、量筒、集气瓶都不能用酒精灯直接加热
d. 配制硫酸溶液时,可先在量筒内加入一定体积的水,再在玻璃棒搅拌下慢慢加入浓硫酸
e.闻气体气味时,应取一瓶盛满气体的集气瓶,稍打开玻璃片,用手轻轻扇地在瓶口扇动,使极少量的气体飘进鼻孔,闻气味
(2)实验室需用1000mL 0.1 mol/L标准Na2CO3溶液,请回答下列问题:
①在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器有 _______ 。
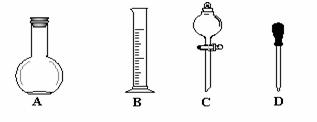
②在容量瓶的使用方法中,下列操作正确的是____________(填写序号)。
a.使用容量瓶前检验是否漏水
b.容量瓶用水洗净后,再用待配溶液洗涤
c.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流注入容量瓶中,然后加蒸馏水。
d.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
③配制1000 mL 0.1 mol·L-1 Na2CO3溶液的实验步骤如下:
a.计算应称取碳酸钠固体的质量为________g。
b.称量碳酸钠固体。
c.将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶。
d.用适量的蒸馏水溶解称量好的碳酸钠固体,冷却。
e.盖好瓶塞,反复上下颠倒,摇匀。
f.继续向容量瓶中加蒸馏水至刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至凹液面与
刻度线相切。
上述步骤的正确操作顺序为_______________________(用序号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,有关金属腐蚀的下列说法不正确的是
A. 钢铁制品腐蚀时正极反应:O2+2H2O+4e-=4OH-
B. 在酸性较强的溶液中,金属主要发生析氢腐蚀
C. 为减缓金属腐蚀,可将要保护的金属物件与外电源的正极相连接
D. 在海轮外壳上附着一些锌块,则可以减缓海轮外壳的腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
利用如图所示装置进行下列实验,能得出相应实验结论的是
| 选项 | ① | ② | ③ | 实验结论 |
|
| A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
| B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 | |
| C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
| D | 稀盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:C>Si |
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W、R是元素周期表前四周期中的常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | 组成蛋白质的基础元素,其最高正化合价与最低负化合价的代数和为2 |
| Y | 地壳中含量最高的元素 |
| Z | 存在质量数为23,中子数为11的核素 |
| W | 生活中大量使用其合金制品,工业上可用电解熔融氧化物的方法制备其单质 |
| R | 有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1) W在元素周期表中的位置为 ; X、Z、W三种元素的原子半径从大到小的顺序是 (用元素符号表示)。
(2) X与氢两元素按原子数目比1:3和2:4构成分子A和B,A的电子式为 ;B的结构式为 ;化合物ZY中存在的化学键类型为 。
(3) 砷(As)是人体必需的微量元素,与X同一主族,As原子比X原子多两个电子层,则砷的原子序数为 ,其最高价氧化物的化学式为 。该族2~4周期元素的气态氢化物的稳定性从大到小的顺序是 (用化学式表示)。
(4) 用RCl3溶液腐蚀铜线路板的离子方程式为 。检验溶液中R3+常用的试剂是 ,可以观察到的现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在足量锌与等物质的量浓度、等体积的盐酸和醋酸反应时,下列叙述正确的是( )
|
| A. | 开始反应时,二者的速率相等 | B. | 盐酸放出的H2多 |
|
| C. | 二者放出的H2一样多 | D. | 醋酸消耗的Zn的质量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验仪器的“0”刻度或实验操作中,与“常规”不同的是
①滴定管 ②品红试纸 ③pH试纸 ④试管中加热NaHCO3 ⑤试管中加热Na2SO4·10H2O制无水硫酸钠 ⑥蒸馏分离I2与CCl4 ⑦用胶头滴管向氢氧化钠溶液中滴加硫酸亚铁溶液制氢氧化亚铁
A.①③④⑥ B.①③⑤⑦ C.②④⑥⑦ D. ①②④⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com