
【题目】下列关于常见有机物的说法正确的是
A. 煤的干馏可得煤油,乙烯和苯能通过石油分馏得到
B. 油脂皂化后可用渗析的方法使高级脂肪酸钠和甘油充分分离
C. 构成蛋白质的基本单元是氨基酸,构成核酸的基本单元是核甘酸
D. 分子式为C3H8O的有机物,发生消去反应能生成2种烯烃
科目:高中化学 来源: 题型:
【题目】比较小麦和家兔体内的各种化学元素( )
A. 种类和含量都相差很大
B. 种类和含量都相差不大
C. 种类相差很大,其中相同元素的含量都大体相同
D. 种类大体相同,其中相同元素的含量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将N2和H2按一定比例混合,在相同状况下其密度是H2密的3.6倍,取0.5mol该混合气体通入密闭容器内,使之发生反应并在一定条件下达到平衡.已知反应达到平衡后容器内压强是相同条件下反应前压强的0.76倍,试求:
(1)反应前混合气体中N2和 H2的体积比为;
(2)达到平衡时混合气体中的氨的体积分数为;
(3)平衡时N2的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用石墨烯和具有粘弹性的聚硅树脂(俗称橡皮泥)制备出一种具有极高 灵敏度的电力学传感材料,能够检测轻微的变形和冲击,其灵敏程度甚至能探测到蜘蛛的运动。该材料可用于制作检测人体脉搏、血压的传感器等。实验室模拟工业合成方法,制备聚硅树脂的中间体氯甲基三乙氧基硅烷ClCH2Si(OEt)3 。量取20mL甲基三氯硅烷(CH3SiCl3)注入三口烧瓶中,开启电磁搅拌加热器升温至66℃,从a中加入浓盐酸,加热A一段时间,待温度升至110℃,停止加热,在三口烧瓶中加入30mL无水乙醇(EtOH),迅速反应生成氯甲基三乙氧基硅烷ClCH2Si(OEt)3,待温度降至室温后,将三口烧瓶中液体转移到蒸馏烧瓶中蒸馏,收集得到174.5℃馏分12mL。
物质 | C2H5OH | CH3SiCl3 | ClCH2SiCl3 | ClCH2Si(OEt)3 |
相对分子质量 | 46 | 149.5 | 184 | 212.5 |
熔点/℃ | -114.1 | -77.8 | — | — |
沸点/℃ | 78.3 | 66.4 | 116.5 | 174 |
密度/g·mL | 0.79 | 1.30 | 1.47 | 1.02 |
已知:甲基三氯硅烷为无色液体,具有刺鼻恶臭,易潮解;氯甲基三乙氧基硅烷易水解,能与碱金属氢氧化物生成碱金属硅醇盐。

(1)连接好装置后,检验装置气密性的操作是:_________________________________;
(2)A装置中发生反应的离子方程式是:_______________________________________;
装置C的作用是:_____________________ ;E中所装液体是:______________;
(3)装置D中发生反应的化学方程式为:① CH3SiCl3 + Cl2 → ClCH2SiCl3 + HCl
②__________________________________________________________________ ;
球形冷凝管的作用是:________________________;
(4)有同学发现该装置有一处不足可能会导致实验失败,应该__________________________________________________;
(5) 该方法制备氯甲基三乙氧基硅烷的产率是:_______________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素周期表的说法正确的是( )
A.短周期是指第一、二、三、四周期
B.周期表中的第五列是第ⅤA族
C.元素周期表中含元素最多的族是第ⅢB族
D.元素周期表有18个族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ksp(CaSO4)=9×10﹣6 , CaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )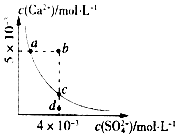
A.在任何溶液中,若有CaSO4沉淀析出,则c(Ca2+)与c(SO42﹣)一定相等
B.d点溶液通过蒸发可以变到c点
C.a点对应的Ksp等于c点对应的Ksp
D.b点将有沉淀生成,平衡后溶液中c(SO42﹣)一定等于3×10﹣3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
(1)甲同学认为,该溶液的pH升高的原因是HCO ![]() 水解程度增大,故碱性增强,该反应的离子方程式为 .
水解程度增大,故碱性增强,该反应的离子方程式为 .
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3 , 并推断Na2CO3的水解程度NaHCO3(填“大于”或“小于”).丙同学认为甲、乙的判断都不充分.
(3)丙认为: 只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则(填“甲”或“乙”)判断正确.试剂X是(填选项).
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
(4)将加热后的溶液冷却到10℃,若溶液的pH8.3(填“大于”“小于”或“等于”),则(填“甲”或“乙”)判断正确.
(5)查阅资料发现NaHCO3的分解温度为150℃,丙断言(填“甲”或“乙”)判断是错误的,理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1gH2和4gO2反应放出71.45kJ热量,则氢气的燃烧热为142.9 kJmol﹣1
B.在稀溶液中,H+(aq)+OH﹣(aq)═H2O(1)△H=﹣57.3 kJmol﹣1 , 若将含0.5molH2SO4的浓硫酸与含1molNaOH的氢氧化钠溶液混合,放出的热量大于57.3kJ
C.HCl和NaOH反应的中和热△H=﹣57.3 kJmol﹣1 , 则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJmol﹣1
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.酸雨是指pH小于7的降水
B.水泥、玻璃、水晶饰物和珍珠都是硅酸盐制品
C.城市空气质量报告中包括PM2.5、SO2、NO2、CO2等污染物
D.钢是用量最大、用途最广的合金,青铜是我国历史上最早使用的合金
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com