
t ℃ 时,将3 mol A和2 mol B气体通入体积为2 L的密闭容器中(容积不变),发生反应:3A(气)+B(气)xC(气),2 min时反应达到平衡状态(温度不变),剩余1.8 mol B,并测得C的浓度为0.4 mol·L-1。请填写下列空白:
(1)x=________;
(2)用A表示该反应的速率为_______mol·L-1·min-1;
(3)若继续向平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是_______(填写下列选项字母序号);
A.化学平衡向正反应方向移动
B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动
D.正、逆反应的化学反应速率将发生同等程度的改变
(4)在t ℃时,若向原平衡混合物中再充入a mol C,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入B_______mol(用含a的式子表示);达到新平衡时,A的物质的量为n(A)= _______ (用含a的式子表示)。
科目:高中化学 来源: 题型:
| 14 |
| 3 |
| 14 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42-、OH- |

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
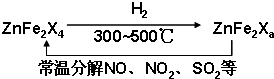
| a |
| Vd-a |
| 1000a |
| 35V |
| 1000b |
| V |
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分)运用化学反应原理研究常见元素的单质及其化合物有重要意义。
(1)合成氨反应N2 (g)+3H2(g) 2NH3(g),△H<0。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡 移动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________(填“增大” “减小” 或“不变”)。
(2)向Na2C2O4溶液加入少量石蕊,溶液显 色,请用离子方程式表示出现该现象的原因: ;
(3)pH相同的氨水和氢氧化钠,分别用蒸馏水稀释至原来溶液的100倍,则稀释后两种溶液的pH分别为m和n,则m n(选填“>”“<”“=”);
(4)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl―NH4Cl为电解质溶液制造新型燃料电池。请写出该电池的正极反应式 。
(5)氢气燃烧热值高。实验测得,在常温常压下,4gH2完全燃烧生成液态水,放出571.6kJ热量,则表示H2燃烧热的热化学方程式为 。
(6)某温度(t℃)时,测得0.01mol・L-1的NaOH溶液的pH=11。在此温度下,将pH=a的H2SO4溶液VaL与pH=b的NaOH溶液VbL混合,若所得混合液为中性,且a+b=12,则Va∶Vb= 。
查看答案和解析>>
科目:高中化学 来源:2014届辽宁省高一下学期期中考试化学试卷(解析版) 题型:实验题
(8分)用一定浓度的稀盐酸与稀NaOH溶液在左下图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。已知强酸与强碱的中和热为57.3KJ/mol,水的比热容为4.2J/(g·℃),有关热量与比热容的计算公式:Q=m×c×△t(Q为热量,m为物质的质量,c为比热容,△t物质温度的变化值)
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是:
(2)将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。

下列叙述正确的是
A.做该实验时环境温度为22 ℃ B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约是1.00 mol/L D.该实验表明有水生成的反应都是放热反应
(3)V1=30mL时HCl和NaOH恰好反应,根据题中所给数据算出的温度变化值约为
(保留整数,计算时可将稀溶液的密度及比热容看成与水近似相同,且溶液混合时体积变化忽略不计);而根据上图的温度变化可读出温度变化值约7 ℃;两者相比所测结果偏低,造成如此现象的原因有:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com