
| 实验步骤 | 实验操作步骤 |
| Ⅰ | 取一定质量的FeCO3固体置于坩埚中,高温煅烧至质量不再减轻,冷却至室温 |
| Ⅱ | 取少量实验步骤Ⅰ所得固体置于一洁净的试管中,用足量的稀硫酸溶解 |
| Ⅲ | 向实验步骤Ⅱ所得溶液中滴加KSCN溶液,溶液变红 |
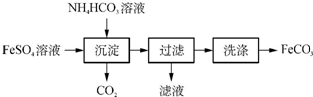
分析 FeSO4溶液中加碳酸氢铵生成CO2、FeCO3,过滤、洗涤,即可得到FeCO3固体,
(1)①FeSO4溶液中加碳酸氢铵发生反应生成CO2、H2O、FeCO3、(NH4)2SO4,结合原子守恒配平书写化学方程式;
②检验铵根离子的方法是利用铵根离子结合氢氧根离子发生反应加热生成氨气,氨气能使湿润的红色石蕊试纸变蓝色;
(2)①三价铁离子可以和硫氰化钾之间反应生成红色的络合物;
②亚铁离子能使高锰酸钾褪色,但是三价铁离子不可以;
(3)①金属铁的氧化物有多种:氧化亚铁、氧化铁、四氧化三铁,根据其中铁元素的价态来回答;
②碳酸铁中的亚铁离子可以被氯水氧化为三价铁离子,铁离子和氢氧化钠反应生成氢氧化铁,氢氧化铁受热分解为氧化铁.
解答 解:(1)①FeSO4溶液中加碳酸氢铵生成CO2、FeCO3,反应的化学方程式为:FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O,
故答案为:FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O;
②检验滤液中含有NH4+的方法是:取少量滤液于试管中,加入足量NaOH溶液,加热,若产生气体可使湿润的红色石蕊试纸变蓝,则滤液中含有NH4+,
故答案为:取少量滤液于试管中,加入足量NaOH溶液,加热,若产生气体可使湿润的红色石蕊试纸变蓝,则滤液中含有NH4+,
(2)①三价铁离子可以和硫氰化钾之间反应生成红色的络合物,发生的反应为:Fe3++3SCN-=Fe(SCN)3,
故答案为:Fe3++3SCN-=Fe(SCN)3;
②亚铁离子能使高锰酸钾褪色,但是三价铁离子不可以,步骤Ⅱ所得溶液中一定含有铁离子,判断是否含有Fe2+,
A.滴加氯水能氧化亚铁离子为铁离子现象不明显,不能鉴别,故A错误;
B.滴加KSCN溶液只能鉴别铁离子的存在,不能证明亚铁离子的存在,故B错误;
C.先滴加KSCN溶液后滴加氯水,弱元溶液中含铁离子,遇到KSCN反应变红色,再滴入氯水不能鉴别溶液中含亚铁离子,故C错误;
D.亚铁离子具有还原性,滴加酸性KMnO4溶液能氧化亚铁离子,若滴入高锰酸钾溶液褪色证明含有亚铁离子,故D正确;
故答案为:D;
(3)①金属铁的氧化物有多种:氧化亚铁、氧化铁、四氧化三铁,氧化亚铁、四氧化三铁中也是含有+2价铁元素的,所以无法确定碳酸亚铁煅烧产物的成分,
故答案为:氧化亚铁、四氧化三铁中也是含有+2价铁元素的;
②碳酸铁可以溶于硫酸,得到硫酸铁、硫酸亚铁等,其中的亚铁离子可以被氯水氧化为三价铁离子,铁离子和氢氧化钠反应生成氢氧化铁,氢氧化铁受热分解为氧化铁,最后过滤,这样可以制得氧化铁,故答案为:氯水;氢氧化钠;过滤.
点评 本题是一道关于金属铁以及化合物的制备、性质的实验方案设计题,要求学生具有分析和解决问题的能力,题目难度中等.


科目:高中化学 来源: 题型:解答题
| 难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
| 沉淀完全时的pH | 11.1 | 6.7 | 9.6 | 3.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
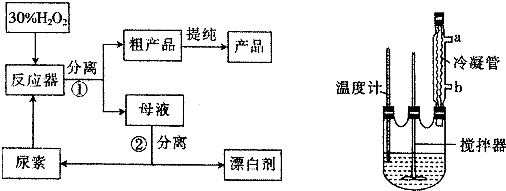
| 分子式 | 外观 | 热分解温度 | 熔点 |
| CO(NH2)2•H2O2 | 白色晶体 | 45℃ | 75~85℃ |
| 实验序号 | 1 | 2 | 3 | |
| KMnO4溶液的体积/mL | 滴定前读数 | 0.00 | 0.00 | 2.00 |
| 滴定后读数 | 19.98 | 20.00 | 22.02 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
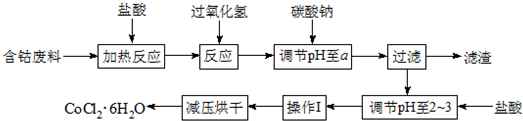
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
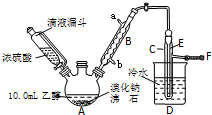 实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):
实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红色液体 |
| 密度/(g•cm-3) | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com