
【题目】已知化合物B是一种红棕色粉末,单质A和单质D是生活中常见的两种金属。它们在一定条件下按下图所示发生转化:

请回答:
(1)上述反应①②③④中属于氧化还原反应的是______________(填写序号)。
(2)写出下列物质化学式:B______,E______,F___________;
(3)将足量的CO2通入E溶液中,离子方程式是_____________________。
(4)H在空气中很容易被氧化成I,该过程的现象是___________________,该反应过程的化学方程式是________________________。
【答案】①②③ Fe2O3 NaAlO2 FeCl2 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- 白色沉淀逐渐变为灰绿色,最终变为红褐色沉淀 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】
化合物B是一种红棕色粉末,则B是氧化铁,混合物A、B加入过量氢氧化钠后,A溶解在氢氧化钠溶液中,则A是铝,反应②是铝与氢氧化钠溶液生成偏铝酸钠和氢气的氧化还原反应;单质铁(D)与盐酸反应生成氯化亚铁,氯化亚铁再与氢氧化钠反应生成氢氧化亚铁(H),氢氧化亚铁经反应①被空气中氧气氧化为氢氧化铁(I),氯化铁溶液(G)经反应③与铁发生氧化还原反应生成F;氯化铝(K)经反应④与氨水反应生成氢氧化铝沉淀。(1)属于氧化还原反应有①②③;B为Fe2O3,E为NaAlO2 ,F为FeCl2;(3)将足量的CO2通入NaAlO2溶液中,离子方程式是:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- ;(4) 氢氧化亚铁,在空气中很容易被氧化成氢氧化铁,4Fe(OH)2+O2+2H2O=4Fe(OH)3,此反应过程可看到白色沉淀逐渐变为灰绿色,最终变为红褐色沉淀。


科目:高中化学 来源: 题型:
【题目】某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是( )
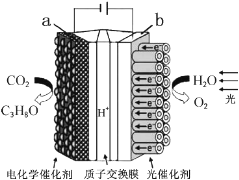
A. 该装置将化学能转化为光能和电能
B. 该装置工作时,H+从b极区向a极区迁移
C. 每生成1molO2,有44g CO2被还原
D. a电极的反应为:3CO2+18H+-18e-=C3H8O+5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、现有下列八种物质: ①铝 ②蔗糖 ③SiO2 ④H2SO4 ⑤NaOH ⑥FeSO4溶液 ⑦Ba(OH)2 ⑧氢氧化铁胶体
(1)上述物质属于电解质的有____________(填序号)。能导电的有__________ (填序号)。
(2)向⑤中加入①的粉末,反应的离子方程式为_____________________。
(3)上述物质中有两种物质在水溶液中反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为__________________________。
(4)实验室制备⑧的离子方程式为:__________________。若在⑧中缓慢加入④的溶液,产生的现象是________________________。
(5) ③是玻璃的主要成分之一,③与⑤溶液反应的化学方程式为____________________。工艺师常用_______(填物质名称)来雕刻玻璃。
II、下列各组物质的分离或提纯,应选用下述方法的哪一种?(填选项字母)
A.分液 B.过滤 C.萃取 D.蒸馏 E.蒸发结晶 F.高温分解
(1)分离CCl4和H2O:___________;
(2)除去澄清石灰水中悬浮的CaCO3: ___________;
(3)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有HA、HB和H2C三种酸。室温下用0.1mol·L-1NaOH溶液分别滴定20.00 mL浓度均为0.1mol·L-1的HA、HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH 溶液体积的变化如图所示。
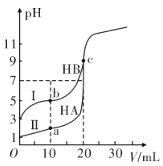
(1)a点时的溶液中由水电离出的c(H+)=________mol·L-1,Ka(HB)=________。
(2)与曲线I 上的c点对应的溶液中各离子浓度由大到小的顺序为________;b点对应的溶液中c(HB)____c(B-)(填“>”“<”或“=”)。
(3)已知常温下向0.1mol·L-1的NaHC 溶液中滴入几滴石蕊试液后溶液变成红色。
①若测得此溶液的pH=1,则NaHC的电离方程式为_______________。
②若在此溶液中能检测到H2C 分子,则此溶液中c(C2-)________c(H2C)(填“>”“<”或“=”)。
③若H2C的一级电离为H2C=H++ HC-,常温下0.1mol·L-1H2C溶液中的c(H+ )=0.11mol·L-1,则0.1mol·L-1NaHC溶液中的c(H+)________0.01mol·L-1(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下 列离子方程式书写正确的是( )
A. 氯气通入水中:Cl2+H2O = 2H++Cl-+ClO-
B. 铁和稀硫酸反应:2Fe+6H+ = 2 Fe3++3H2↑
C. 碳酸钙与醋酸反应:CaCO3+2H+ = Ca2++CO2↑+H2O
D. 氢氧化铝和氢氧化钠溶液反应:Al(OH)3+OH- = AlO2-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人被蚂蟥叮咬后伤口处常流血不止,科学家希望从蚂蟥体内提取某种药物,该药物具有
A. 止血性能 B. 抗血凝性能 C. 止痛、止痒性能 D. 抗过敏性能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有以下6个反应(反应条件略):
A.2Na+2H2O ═2NaOH+H2↑ B.CH4+2O2 ![]() CO2+2H2O
CO2+2H2O
C.KClO3![]() 2KCl+3O2↑ D.CaCO3+2HCl═CaCl2+H2O+CO2↑
2KCl+3O2↑ D.CaCO3+2HCl═CaCl2+H2O+CO2↑
E.Na2O+CO2 ═Na2CO3 F.CO2+C![]() 2CO
2CO
既属于化合反应又属于氧化还原反应的有__________(填编号,下同),不属于氧化还原反应的有__________.
(2)根据反应:①2Fe3++2I-===2Fe2++I2,②Br2+2Fe2+===2Fe3++2Br-,③ Br2+2I-===I2+2Br-,回答下列问题。
①试判断离子的还原性由强到弱的顺序是________
A.Br-、Fe2+、I- B.I-、Fe2+、Br- C.Br-、I-、Fe2+ D.Fe2+、I-、Br-
②某溶液中含有Br-、Fe2+、I-,为了氧化I-而不影响Br-和Fe2+,选用的氧化剂是__________;
③I2与Br-能否发生反应________
A.能 B.不能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种医药中间体,常用于制备抗凝血药。可以通过如图所示的路线合成:
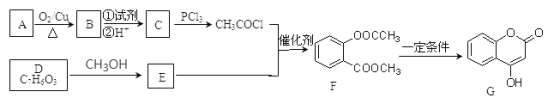
已知:①RCOOH![]() RCOCl;②D与FeCl3溶液能发生显色反应。
RCOCl;②D与FeCl3溶液能发生显色反应。
③:![]()
回答下列问题:
(1)C→H的反应类型是_______________,B→C步骤①中所加的试剂可能是_____________,D中的官能团名称为____________________。
(2)B、E的结构简式为:B:_____________,E:______________。
(3)A→B的化学方程式为_________________,G与足量NaOH溶液充分反应的化学方程式为_________________________。
(4)写出同时满足下列条件的所有E的同分异构体的结构简式________________。
①不能发生水解反应,能发生银镜反应
②该分子核磁共振氢谱有五个组峰,且峰面积之比为2:2:2:1:1
③与FeCl3溶液能发生显色反应
④苯环上有两种不同化学环境的氢原子
(5)已知:酚羟基一般不易直接与羧酸酯化。苯甲酸苯酚酯(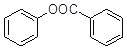 )是一种重要的有机合成中间体。试结合题中信息写出以苯酚、甲苯为原料制取该化合物合成路线流程图(其他试剂任选)______。合成路线流程图示例:
)是一种重要的有机合成中间体。试结合题中信息写出以苯酚、甲苯为原料制取该化合物合成路线流程图(其他试剂任选)______。合成路线流程图示例:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com