
| A. | CO2分子的结构式:O=C=O | |
| B. | S2-的结构示意图: | |
| C. | R2+离子核外有a个电子,b个中子,R原子符号为:${\;}_{a+2}^{a+b+2}$R | |
| D. | 次氯酸的电子式: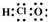 |
分析 A.二氧化碳分子中碳原子和每个氧原子之间共用两个电子对;
B.硫离子核外有3个电子层,最外层有8个电子;
C.元素符合左下角的数字表示质子数,左上角数字表示质量数;
D.次氯酸的中心原子是氧原子,分子中存在1个氢氧键和1个氧氯键.
解答 解:A.二氧化碳分子中碳原子和每个氧原子之间共用两个电子对,所以其结构式为:O=C=O,故A正确;
B.硫离子核外有3个电子层,最外层有8个电子,其离子结构示意图为: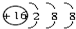 ,故B正确;
,故B正确;
C.R2+离子核外有a个电子,b个中子,则R原子的质子数为a+2,质量数为a+b+2,R原子符号为:${\;}_{a+2}^{a+b+2}$R,故C正确;
D.次氯酸的中心原子为O原子,次氯酸的电子式为: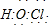 ,故D错误;
,故D错误;
故选D.
点评 本题考查了化学用语的表示方法,题目难度中等,注意掌握离子结构示意图、元素符号、结构式、电子式的概念及书写原则,D为易错点,需要明确次氯酸的中心原子为O原子.


科目:高中化学 来源: 题型:选择题
| A. | 共价化合物中一定不含有离子键,离子化合物中可能含有共价键 | |
| B. | 一定条件下,将1 mol N2与3 mol H2充入密闭容器中充分反应可生成2 mol NH3 | |
| C. | 充电电池的化学反应原理是氧化还原反应 | |
| D. | Na2O和Na2O2晶体中阳离子与阴离子个数比均为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 反应方程式中的x=1,30min时改变条件后,A的转化率将变减小 | |
| B. | 前30 min内 A的反应速率为0.05 mol/(L•min) | |
| C. | 20至40 min内表示处于平衡状态,该反应为放热反应 | |
| D. | 30 min时改变的条件是加入负催化剂,40 min时改变的条件是升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向海水中加入明矾可以使海水淡化,用于解决淡水供应危机 | |
| B. | 将地沟油回收再加工为食用油,以减缓水体富营养化 | |
| C. | 大力推广农作物的生物防治技术,以减少农药的使用 | |
| D. | 用聚氯乙烯代替木材,生产包装盒、快餐盒等,以减少木材的使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
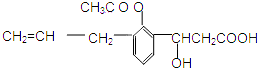
| A. | 可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和 | |
| B. | 该物质1mol与足量NaOH溶液反应,消耗NaOH的物质的量为2mol | |
| C. | 可与氯化铁溶液发生显色反应 | |
| D. | 该有机物属于芳香烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与氯气反应 | B. | 次氯酸的分解 | ||
| C. | 乙醇与乙酸的酯化反应 | D. | 甲烷与氧气的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有CO2和SO2 | B. | 可能有HBr、CO2 | ||
| C. | 肯定没有HBr、H2S、HCl | D. | 以上结论均不正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com