
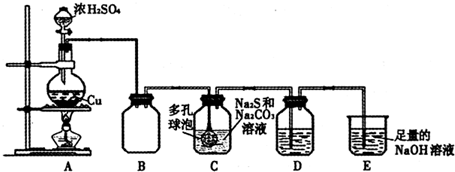
���� ����Ʊ�Na2S2O3•5H2O��Aװ�ã��ڼ��������£�Cu��Ũ���ᷴӦ��������ͭ�����������ˮ���䷴Ӧ�ķ���ʽΪ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��Bװ�ã�����ƿ����ֹCҺ�嵹����Aװ�ã�Cװ�ã�ΪNa2S2O3������װ�ã�������ݿ���������������Һ�ĽӴ������ʹ���屻������գ����������ʵ���ȷ�ȣ�2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2��Dװ�ã����������ܺ�Ʒ�����ã����������ܱ�������������������嵥�ʣ�������Һ����ɫ��ʢ��Ʒ�졢��ˮ��KMnO4��Һ���������Ǽ���װ��B��SO2������Ч�ʣ�Eװ�ã����������ж�������ֱ���ŷŵ������У�β������װ�ã�����δ��Ӧ�Ķ�������
��1�����������Ľṹ�ص��жϣ���װ���ص�Ϊ�ڼ��������£�Cu��Ũ���ᷴӦ��������ͭ�����������ˮ�����ڹ�Һ������װ�ã�ʵ���һ�������Aװ����ȡ������Ũ��������������ڼ��������·�Ӧ�����������Ȼ��̺�ˮ��
��2����Dװ�ü�����������Ƿ���ȫ���գ����ݶ�������Ļ�ԭ�Ժ�Ư���Է�����
��3������Ʒ���Ƿ����Na2SO4���ȼ������ų����ţ��������Ȼ���������������ӣ�
��4������Na2S2O3�������I2���ٸ���K2Cr2O7��I2�Ĺ�ϵ���K2Cr2O7�����ʵ�����Ũ�ȣ�
��� �⣺��1�����������Ľṹ�ص��֪��װ��A�еμ�Ũ��������������Ƿ�Һ©����װ��AΪ�����������ȡ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O����װ�����ڹ�Һ������װ�ã�ʵ���һ�������Aװ����ȡ������Ũ��������������ڼ��������·�Ӧ�Ʊ�Cl2�����ӷ���ʽΪ��MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++2H2O+Cl2����
�ʴ�Ϊ����Һ©����MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++2H2O+Cl2����
��2��װ��D�������Ǽ���װ��C��SO2������Ч�ʣ�˵��D�����������������Ӧ���������Ե��������������Ư���ԣ���ʹƷ����ɫ�����л�ԭ�ԣ��ܱ���ˮ��������ˮ��ɫ��SO2+Br2+2H2O=H2SO4+2HBr��������������������Һ����������ԭ��Ӧ����Ԫ�ػ��ϼ����ߣ�����������ֻ�ԭ�ԣ����������Һ��ɫ��5SO2+2KMnO4+2H2O=K2SO4+2MnSO4 +2H2SO4�����Կ�����Ʒ�졢��ˮ��KMnO4��Һ����������������Ƿ���ȫƷ�����գ���C��SO2����Ч�ʵͣ���D�н���϶�Ķ���������D����Һ��ɫ�ܿ���ɫ��
�ʴ�Ϊ��Ʒ�졢��ˮ��KMnO4��Һ�� ��Һ��ɫ�ܿ���ɫ��
��3�����Na2S2O3•5H2O��Ʒ���Ƿ����Na2SO4���ʣ��ȼӹ�����ϡ�����ų����ţ����ã�ȡ�ϲ���Һ���ټ��Ȼ����������ְ�ɫ������˵����Һ�к�����������ӣ���Na2S2O3•5H2O��Ʒ�к���Na2SO4��
�ʴ�Ϊ��ȡ������Ʒ��������ϡ�����У����ã�ȡ�ϲ���Һ������˺�ȡ��Һ�����μ�BaCl2��Һ�������ְ�ɫ������˵��Na2S2O3•5H2O�����к���Na2SO4���ʣ�
��4��10.00mL K2Cr2O7��Һ����ƿ�У��������KI�����������ϡH2SO4����Ӧ����I2����0.1000mol•L-1 Na2S2O3����Һ�ζ����յ㣬3��ƽ��ʵ����ƽ������Na2S2O3��Һ�����Ϊ30.00mL����n��Na2S2O3��=cV=0.1000mol•L-1��0.0300L=0.00300mol��
��֪��Cr2O72-+6I-+14H+�T2Cr3++3I2+7H2O��2S2O32-+I2�TS4O62-+2I-��
Cr2O72-������3I2������6S2O32-
1mol 6mol
n 0.00300mol
��n��K2Cr2O7��=0.000500mol ����c��K2Cr2O7��=$\frac{0.000500mol}{0.01L}$=0.0500mol/L��
�ʴ�Ϊ��0.0500��
���� ��������Ļ����������Ϊ���壬���������ʵ��Ʊ�������ơ�������ԭ�ζ���Ӧ�á�ʵ�������������ѧ����ȣ��Ѷ��еȣ��Ƕ�֪ʶ���ۺ����������������������Ŀ��飬ע�����ù�ϵʽ���м��㣮


 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �����Ӿ��������� | B�� | �嵥���������� | ||
| C�� | �÷�Ӧ���ڸ��ֽⷴӦ | D�� | ��Ԫ�صķǽ����Ա���Ԫ��ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ϊ1.8NA | B�� | ������Ϊ0.1NA | C�� | ������Ϊ2NA | D�� | ԭ����Ϊ2.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
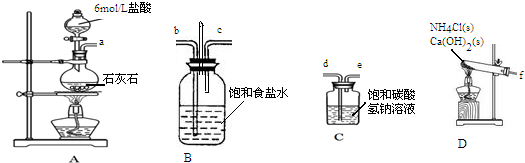 �Ʊ�̼�����ƣ�Ȼ����̼�������Ʊ�̼���ƣ�
�Ʊ�̼�����ƣ�Ȼ����̼�������Ʊ�̼���ƣ�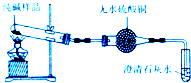
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
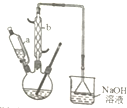 �������Ǻϳ�����-66����Ҫԭ��֮һ��ʵ���Һϳɼ������ԭ�����й����ݼ�װ��ʾ��ͼ���£�
�������Ǻϳ�����-66����Ҫԭ��֮һ��ʵ���Һϳɼ������ԭ�����й����ݼ�װ��ʾ��ͼ���£�
| ���� | �ܶȣ�20�棩 | �۵� | �е� | �ܽ��� |
| ������ | 0.962g/cm3 | 25.9�� | 160.8�� | 20��ʱˮ���ܽ��Ϊ3.6g���ɻ������Ҵ����� |
| ������ | 1.360g/cm3 | 152�� | 337.5�� | ��ˮ�е��ܽ�ȣ�15��ʱ1.44g��25��ʱ2.3g���������Ҵ��������ڱ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ʳ��ά����ͻ���ı������ܣ�������ġ�����Ӫ���ء���ľ������һ�ַ�������ʳ��ά���䵥��֮һ--���Ӵ��ṹ��ʽ��ͼ��ʾ�������йؽ��Ӵ���˵����ȷ���ǣ�������
��ʳ��ά����ͻ���ı������ܣ�������ġ�����Ӫ���ء���ľ������һ�ַ�������ʳ��ά���䵥��֮һ--���Ӵ��ṹ��ʽ��ͼ��ʾ�������йؽ��Ӵ���˵����ȷ���ǣ�������| A�� | ���Ӵ������������ֺ��������� | |
| B�� | ���Ӵ�����������̼ԭ�Ӳ�������ͬһƽ���� | |
| C�� | ���Ӵ�������Ũ��ˮ��Ӧ���������3 mol Br2 | |
| D�� | ���Ӵ��ܷ����ķ�Ӧ��������������ԭ��ȡ�����ӳɡ��ۺ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ���� | п��״̬ | ��Ӧ�¶�/�� | �ռ�100mL��������ʱ��/s |
| �� | ��Ƭ | 15 | 200 |
| �� | ��Ƭ | 25 | 90 |
| �� | ��ĩ | 25 | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O22-��S2-������ͬ���������͵����� | |
| B�� | H��D��T��Ϊͬλ�أ�H2O��D2O��T2O��Ϊͬ�������� | |
| C�� | �����Ԫ����ָ IA�������Ԫ�� | |
| D�� | ���ڱ��е�15��Ԫ�ص�����������Ӧˮ����Ļ�ѧʽ��ΪH3RO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶X��Y��Z | |
| B�� | ����������ˮ�������Դ�ǿ������˳����HXO4��H2YO4��H3ZO4 | |
| C�� | ��̬�⻯����ȶ���X��Y��Z˳��������ǿ | |
| D�� | �����ӵ�������Z��Y��X˳����ǿ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com