
| A. | 固态Na2O2和熔融态NaHSO4中的阴、阳离子个数比均为1:1 | |
| B. | 离子化合物中一定不含共价键 | |
| C. | 某主族元素的最高价含氧酸为HnROm,则其气态氢化物一般是H8-2m+nR或RH8-2m+n | |
| D. | 元素周期表中L层电子为奇数的元素的化合价也都是奇数 |
分析 A、固态Na2O2中含有钠离子和过氧根离子;NaHSO4晶体中含有1个Na+和1个HSO4-;
B、离子化合物中可能含共价键;
C、化合物中元素的化合价代数和为零,据此计算X元素的化合价,再利用最高正化合价+|最低负化合价|=8,计算X元素在气态氢化物中的化合价;
D、L层电子为奇数,说明第二周期没排满,该元素在第二周期,再根据主族元素的化合价与其最外层电子数之间的关系判断.
解答 解:A、固态Na2O2中含有钠离子和过氧根离子,阴、阳离子个数比均为1:2;NaHSO4晶体中含有1个Na+和1个,NaHSO4晶体HSO4-中的阴、阳离子个数比均为1:1,故A错误;
B、离子化合物中可能含共价键,故B错误;
C、R的最高价含氧酸分子式为HnROm,化合物HnROm中各元素的化合价代数和为零,令R元素的化合价为a,则:(+1)×n+a+(-2)m=0,解得,a=2m-n,根据最高正化合价+|最低负化合价|=8可知,所以氢化物中化合价为最低化合价-(8-2m+n);根据化合物中各元素的化合价代数和为零可知,(+1)x+[-(8-2m+n)]=0,解得x=8-2m+n,则气态氢化物一般是H8-2m+nR或RH8-2m+n,故C正确;
D.L层电子为奇数,说明第二周期没排满,该元素在第二周期,L为奇数分别为1、3、5、7分别为锂、硼、氮、氟,L层电子为奇数的元素的化合价不一定也都是奇数,如其中的氮元素的化合价有+1、+2、+3、+4、+5,故D错误;
故选C.
点评 本题考查了离子晶体的构成、离子键、化合物中元素化合价的计算、原子结构与元素周期表,题目难度不大,注意常见主族的化合价.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯化氢的摩尔质量等于NA个氯化氢分子的质量 | |
| B. | 常温常压下1mol二氧化碳的体积大于22.4L | |
| C. | 64g金属铜发生氧化反应,一定失去2NA个电子 | |
| D. | 62g氧化钠溶于水后,所得溶液中含有NA个O2-离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
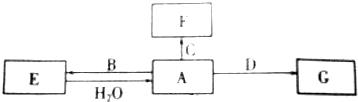
 ,写出E与H2O反应生成A的化学方程式2Na2O2+2H2O=4NaOH+O2↑
,写出E与H2O反应生成A的化学方程式2Na2O2+2H2O=4NaOH+O2↑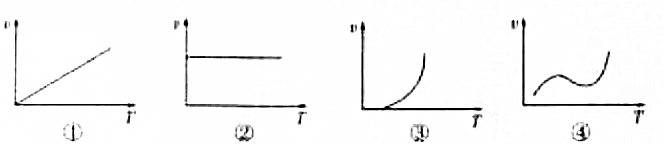
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石头纸(主要成分CaCO3)代替普通纸,减少对木材的使用 | |
| B. | 合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺的状况 | |
| C. | 将秸秆充分燃烧,避免秸秆腐烂造成环境污染 | |
| D. | 推广碳捕集和储存技术,逐步实现二氧化碳零排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 ,其阴、阳离子的个数之比为1:2.
,其阴、阳离子的个数之比为1:2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
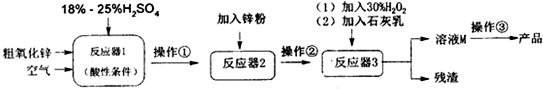
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
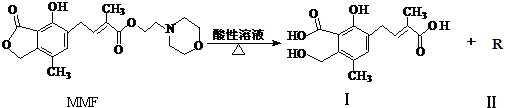
| A. | MMF分子中含有三种官能团 | |
| B. | 可以用NaHCO3溶液区别MMF与化合物Ⅰ | |
| C. | 化合物Ⅱ分子中只含碳、氢元素,属于烃类 | |
| D. | 1 mol MMF与足量NaOH 溶液共热,最多可消耗4 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝的金属性比镓强,铝的熔点比镓低 | |
| B. | 铝表面形成致密的氧化膜,所以可以用铝制容器来腌制咸菜 | |
| C. | Ga(OH)3与Al(OH)3性质相似,一定能与NaOH溶液反应 | |
| D. | 铝镓合金与水反应后的物质可以回收利用冶炼铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com