



科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
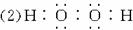
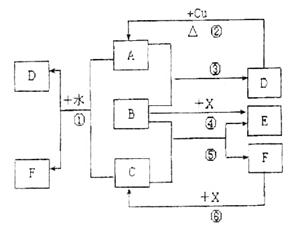
(1)根据上图中的信息,B、C、D、X氧化性从强到弱的顺序是________________________。
(用对应物质的化学式表示)
(2)B的电子式为________________________ 。
(3)写出反应②的化学方程式______________________________________________。
(4)写出反应①⑥的离子方程式:
①______________________________________________________________;
⑥______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013届辽宁省铁岭市六校协作高三第三次联合考试化学试卷(带解析) 题型:填空题
(10分)已知A~F是中学化学常见的物质,其中A、C、E为气体,B、D为液体,D是一种不挥发性酸,其浓溶液有强氧化性,F的溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子,实验室常用B和X制备单质E。反应中部分生成物已略去。试回答下列问题:
(1)写出B的电子式 ,化学键类型 。
(2)根据图中信息,B、C、X氧化性从强到弱的顺序是________________________。
(3)X与铝高温下反应的方程式为______________。
(4)写出反应②的化学方程式_____________。
(5)反应①的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁省铁岭市六校协作高三第三次联合考试化学试卷(解析版) 题型:填空题
(10分)已知A~F是中学化学常见的物质,其中A、C、E为气体,B、D为液体,D是一种不挥发性酸,其浓溶液有强氧化性,F的溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子,实验室常用B和X制备单质E。反应中部分生成物已略去。试回答下列问题:
(1)写出B的电子式 ,化学键类型 。
(2)根据图中信息,B、C、X氧化性从强到弱的顺序是________________________。
(3)X与铝高温下反应的方程式为______________。
(4)写出反应②的化学方程式_____________。
(5)反应①的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com