
【题目】在容量瓶上无需标出的是
A.刻度线 B.容量标准 C.温度 D.配制溶液的浓度
科目:高中化学 来源: 题型:
【题目】实验室用 KMnO4 与密度为 1.19 g·cm-3,溶质质量分数为 36.5%的 HCl 溶液反应制取氯气,反应方程式为:
2KMnO4 + 16HCl = 2KCl + 2MnCl 2 + 5Cl 2↑ + 8H2O
(1)用双桥线法分析电子转移的方向和数目____________(直接在上述方程式中表示);
(2)氧化剂_____________ 氧化产物________________
(3)若反应中有 0.5 mol 电子转移,被氧化的 HCl 的物质的量是__________ mol;
(4)c(HCl)=_________________________________ ;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤能排放大量的CO、CO2、SO2,PM2.5(可入肺颗粒物)。污染跟冬季燃煤密切相关,SO2. CO、CO2也是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
(1)工业上可用CO2和H2反应合成甲醇。已知25°C、101 kPa下:
H2(g)+1/2O2(g)=H2O (g) △H1=—242kJ/mol
CH3OH+3/2O2(g) =CO2(g)+2H2O △H2=—676kJ/mol
写出CO2与H2反应生成CH3OH(g)与H2O (g)的热化学方程式_________________。
(2)工业上还可以通过下列反应制备甲醇:CO (g) +2H2 (g)![]() CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。

①下列说法不能判断该反应达到化学平衡状态的是____(填字母)。
a. H2的消耗速率等于CH3OH的生成速率的2倍
b.H2的体积分数不再改变
c.体系中H2的转化率和CO的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA____PB(填“>”“<”或“=’’)。
③若达到化学平衡状态A时,容器的体积为20 L。如果反应开始时仍充入10 mol CO和20molH2,则在平衡状态B时容器的体积V(B)=________L。
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:
① 该电池的负极反应:___________________;
②当甲中消耗2.24LO2(标准状况)时,乙中a极增重____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:

(1)请写出Fe2O3与①反应的离子方程式______________________________。
(2)物质②为_______________。
(3)请写出FeCl3与铁粉反应的化学方程式________________________。
(4)向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为____________ ,此过程中发生的氧化还原反应为(用化学方程式表达)_________________________。
(5)将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③__________________,它与FeCl3溶液、Fe(OH)3浊液的本质区别是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图所示的装置蒸馏海水,下列说法正确的是( )

A. 实验时冷却水应从a进入,从b流出
B. 蒸馏烧瓶中要加入碎瓷片,目的是防止暴沸
C. 锥形瓶中能收集到高浓度的氯化钠溶液
D. 该装置可用于分离海水中的NaCl和MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是

A. 元素X与元素Z的最高正化合价之和的数值等于8
B. 原子半径的大小顺序为:rX>rY>rZ>rW>rQ
C. 离子Y2-和Z3+的核外电子数和电子层数都不相同
D. 元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【衡阳市2017届下学期第三次联考】石油分馈得到的轻质油可通过Pt催化重整脱氢环化,逐步转化为芳香烃。以链烃A为原料合成两种髙分子材料的路线如下:
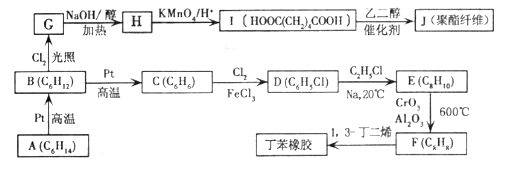
已知以下信息:
①B的核磁共振氢谱中只有一组峰;G为一氯代烃。
②R—X+R′—X![]() R—R′(X为卤素原子,R、R'为烃基)
R—R′(X为卤素原子,R、R'为烃基)
回答以下问题:
(1)B的名称为_______;由F生成丁苯橡胶的反应类型是______________。
(2)E分子中最多有____个原子共面;J的结构简式为_______。
(3)由G生成H的化学方程式为___________________。
(4)I的同分异构体中,能同时满足下列条件的结构共有____种(不含立体异构)。
①能与饱和NaHCO3溶液反应产生气体;
②既能发生银镜反应,又能发生水解反应。
其中核磁共振氢谱为4组峰,且面积比为6: 2:1:1的是_____ (写出其中一种的结构简式)。
(5)参照上述合成路线,以2 -甲基己烷和一氯甲烷为原料(无机试剂任选),设计制备化合物E的合成路线:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六氟化硫分子(如下图)呈正八面体,难以水解,在电器工业方面有着广泛用途。下列有关SF6的推测正确的是( )

A. SF6易燃烧生成二氧化硫
B. SF6是极性分子
C. SF6中各原子均达到 8 电子稳定结构
D. 高温条件下,SF6微弱水解生成H2SO4和HF
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com