
| A、在加热搅拌条件下加入MgO,可除去MgCl2溶液中的Fe3+ |
| B、pH=4.5的番茄汁中c(H+ )是pH=6.5的牛奶中c(H+)的100倍 |
| C、常温下,CH3COONa和CH3COOH的混合溶液中(pH=7):C(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
| D、常温下,Cd(OH)2和Co(OH)2的混合悬浊液中,c(Cd2+)是c(Co2+)的3.5倍,已知:KSP(Cd(OH)2)=7.2×10-15,Ksp(Co(OH)2)=1.8×10-15 |


科目:高中化学 来源: 题型:
| A、①②⑤ | B、①③⑥ |
| C、②④⑤ | D、①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
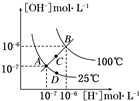
| A、图中四点KW间的关系:A=D<C<B |
| B、若从A点到C点,可采用温度不变在水中加少量CH3COONa固体 |
| C、若从A点到D点,可采用温度不变在水中加少量酸 |
| D、若处在B点所在的温度,将pH=2的硫酸与pH=10的NaOH的两种溶液等体积混合后,溶液显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
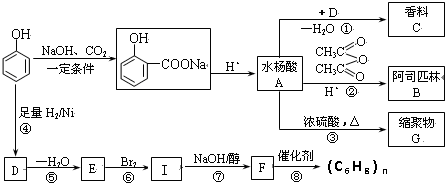
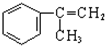 丙:分子式C9H8O,(部分性质,能使Br2/CCl4褪色 )由甲出发合成丙的路线之一如下:
丙:分子式C9H8O,(部分性质,能使Br2/CCl4褪色 )由甲出发合成丙的路线之一如下: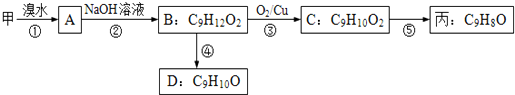
查看答案和解析>>
科目:高中化学 来源: 题型:
A、乙醇与浓氢溴酸反应:CH3CH2OH+HBr
| |||
B、溴乙烷与氢氧化钠溶液共热:CH3CH2HBr+NaOH
| |||
C、苯酚钠中通入二氧化碳2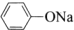 +CO2+H2O→ +CO2+H2O→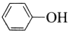 +Na2CO3 +Na2CO3 | |||
D、蔗糖在稀硫酸作用下水解:C12H22O11(蔗糖)+H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
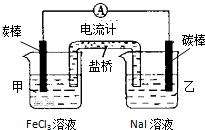
| A、反应开始时,乙中石墨电极上发生氧化反应 |
| B、反应开始时,甲中石墨电极上Fe3+被还原 |
| C、电流计读数为零时,反应达到化学平衡状态 |
| D、电流计读数为零后,在甲中溶入FeCl2固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com