
【题目】某有机物的分子式为C5H10O,它能发生银镜反应,若将它与H2加成,所得产物的结构简式可能的一组是
①(CH3)3CCH2OH ②(CH3CH2)2CHOH ③ CH3CH2C(CH3)2OH ④CH3(CH2)3CH2OH
A. ①② B. ②③ C. ②④ D. ①④
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铁单质及其化合物在生活生产中应用广泛。
(1)硫酸铁可作絮凝剂,常用于净水,其原理是(用离子方程式表示)______________________。
(2)已知25°C时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+![]() Fe3++3H2O的平衡常数K=______________
Fe3++3H2O的平衡常数K=______________
(3)电浮选凝聚法是工业上采用的一种污水处理方法,保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某研究小组设计装置如图所示。

①装置B中通入空气的电极反应是_______________
②装置A中,阳极的电极反应式分别为Fe-2e-=Fe2+、_______________
③实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣.此时,应向污水中加入适量的___________
a.H2SO4b.BaSO4c.Na2SO4d.NaOHe.CH3CH2OH
(4)工业催化剂K3[Fe(C2O4)3]·3H2O是翠绿色晶体,在421~553℃时,分解为Fe2O3、K2CO3、CO、CO2、H2O。实验室由草酸亚铁晶体(FeC2O4·2H2O)、草酸钾(K2C2O4)、草酸(H2C2O4)和双氧水(H2O2)混合制备。
①制备过程要防止草酸被H2O2氧化,请写出草酸被H2O2氧化的化学方程式__________________。
②配合物的稳定性可以用稳定常数K来衡量,如Cu2+ + 4NH3![]() [Cu(NH3)4]2+,其稳定常数表达式为:
[Cu(NH3)4]2+,其稳定常数表达式为:![]() 。已知:[Fe(C2O4)3]3-的稳定常数K1=1020, Fe(SCN)3的稳定常数K2=2×103,请设计检验K3[Fe(C2O4)3]·3H2O中铁元素的方案_______________________。
。已知:[Fe(C2O4)3]3-的稳定常数K1=1020, Fe(SCN)3的稳定常数K2=2×103,请设计检验K3[Fe(C2O4)3]·3H2O中铁元素的方案_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是( )

A. 含有M元素的化合物均可与强酸、强碱反应
B. 原子半径Z<X<M
C. Z2与Z3互为同素异形体
D. Y的最高价氧化物对应水化物的酸性比X的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要使蛋白质从溶液中析出,而又不改变它的性质,应加入( )
A. 饱和(NH4)2SO4溶液 B. 稀NaOH溶液 C. 饱和CuSO4溶液 D. 乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分物质和条件己略去)。A是由两种元素组成的难溶于水的物质,摩尔质量为88 g·mol-l;B是常见的强酸;C是一种气态氢化物;气体E能使带火星的木条复燃;F是最常见的无色液体;无色气体G能使品红溶液褪色;向含有I的溶液中滴加KSCN试剂,溶液出现血红色。请回答下列问题:

(1)G的化学式为_________________________。
(2)C的电子式为________________________。
(3)写出反应①的离子方程式:_____________________。
(4)写出反应②的化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合肼(N2H4·H2O)又名水合联氨,无色透明,具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂。利用尿素法生产水合肼的原理为:CO(NH2)2+2NaOH+NaC1O=Na2CO3+N2H4·H2O+NaCl
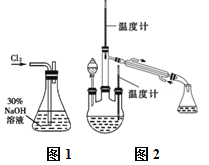
实验一:制备NaClO溶液。(实验装置如图1所示)
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外还有______(填标号)。
A.玻璃棒 B.烧杯 C.烧瓶 D.容量瓶 E.胶头滴管
(2)锥形瓶中发生反应的离子方程式是___________________。
实验二:制取水合肼。(实验装置如图2所示)
(3)①仪器A的名称为_______________。
②反应过程中需控制反应温度,同时将分液漏斗中溶液缓慢滴入A中,如果滴速过快则会导致产品产率降低,同时产生大量氮气,写出该过程的化学反应方程式:__________,故分液漏斗中的溶液是______(填标号)。
A.CO(NH2)2溶液 B.NaOH和NaClO
③充分反应后,加热蒸馏A内的溶液,收集108~114℃馏分,即可得到水合肼的粗产品。
实验三:测定馏分中肼含量。
(4)称取馏分5.0g,加入适量NaHCO3固体,加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加23滴淀粉溶液,用0.10mol·L-1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右。(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)
①滴定时,碘的标准溶液盛放在______(填"酸式”或“碱式”)滴定管中,本实验滴定终点的现象为____________________。
②实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4·H2O)的质重分数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某元素+3价离子的电子排布式为1s22s22p63s23p63d3,该元素在周期表中的位置和区域是( )
A. 第三周期第ⅥB族;p区B. 第三周期第ⅢB族;ds区
C. 第四周期第ⅥB族;d区D. 第四周期第ⅢB族;f区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CH3CH3→CH3CH2Cl→CH2= CH2→CH3CH2OH的转化过程中,经过的反应是
A. 取代→消去→加成 B. 裂解→取代→消去
C. 取代→加成→氧化 D. 取代→消去→水解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com