
| A. | NaOH溶液可保存在玻璃塞的试剂瓶中 | |
| B. | 液溴应盛放在用水密封且用玻璃塞塞紧的棕色试剂瓶中 | |
| C. | 用pH试纸无法测得某氯水的pH值,因为氯水具有漂白性 | |
| D. | SO2能使紫色KMnO4溶液褪色,是由于其具有漂白性 |
分析 A.玻璃中含有SiO2能与碱反应有黏性的Na2SiO3;
B.溴水见光易分解,用棕色瓶盛装;
C.氯水为氯气的水溶液,显酸性,其中的次氯酸有漂白性;
D.SO2可使酸性KMnO4溶液褪色,发生氧化还原反应.
解答 解:A.因玻璃中含有SiO2,SiO2能与碱反应SiO2+2NaOH═Na2SiO3 +H2O,生成有黏性的Na2SiO3,会导致玻璃塞打不开,所以装浓NaOH溶液的试剂瓶不能用玻璃塞密封,故A错误;
B.液溴应盛放在用水密封且用玻璃塞塞紧的棕色试剂瓶中液溴容易挥发,所以要密封保存,且会加入少量的水密封.在水中有:Br2+H2O?HBr+HBrO,加热或光照,都会促进反应.所以,要避光,用棕色的瓶子.但是由于溴水溶液呈酸性,会腐蚀橡胶塞,所以,只能用玻璃塞,故B正确;
C.氯水为氯气的水溶液,显酸性,其中的次氯酸有漂白性,不能用pH试纸测,故C错误;
D.SO2可使酸性KMnO4溶液褪色,发生氧化还原反应,S元素的化合价升高,体现其还原性,故D错误.
故选B.
点评 本题考查化学试剂的存放、PH试纸的使用、氧化还原反应,难度不大,注意在学习中加强基础知识的积累.


科目:高中化学 来源: 题型:解答题
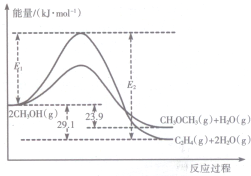 醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应:
醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4molA+2molB | B. | 1molA+0.5molB+1.5molC | ||
| C. | 3molC+1molB | D. | 3molC+2molA+1molB |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
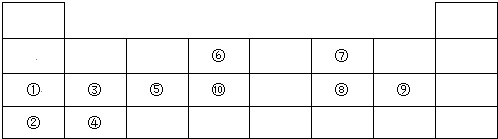
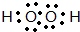 ,⑩与⑨形成的5原子分子的结构式为
,⑩与⑨形成的5原子分子的结构式为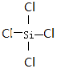 .
.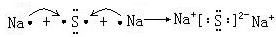 ,氢化物X与化合物Y发生反应的离子方程式为S2-+H2O2=S↓+2OH-.
,氢化物X与化合物Y发生反应的离子方程式为S2-+H2O2=S↓+2OH-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com