
| A. | K+MnO4- Cl- SO42- | B. | Na+K+NH4+Ba2+ | ||
| C. | Na+HCO3- NO3- SO42- | D. | Na+SO42- S2- Cl- |
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:解答题

| 沉淀物 | 开始沉淀 | 完全沉淀 |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤时玻璃棒与三层滤纸的一边接触 | |
| B. | 过滤时漏斗下方紧贴烧杯内壁 | |
| C. | 加热试管内物质时,试管底部与酒精灯灯芯接触 | |
| D. | 加热氯酸钾制取氧气结束时,先从水槽中移出导气管,再熄灭酒精灯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验序号 | 实验步骤(内容) | 现象 |
| ① | 在贴有标签a、b的试管中分别加入1.0 g Na2CO3固体和NaHCO3固体,观察外观. | / |
| ② | 分别滴入几滴水,振荡,摸试管底部. | 试管 a吸热现象更明显(填“a”或“b”) |
| ③ | 继续向两试管中分别加入10.0 mL水,用力振荡,观察现象. | / |
| ④ | 再分别向两试管中滴加2滴酚酞溶液,观察现象. | 溶液均变红,颜色较深的试管是 a(填“a”或“b”). |
| ⑤ | 最后分别向两溶液中滴加足量盐酸. | 红色褪去,均有无色气体产生.经计算生成气体的是a <b(填“>”“<”或“=”) |
| ⑥ | 加热大试管一段时间.(注:棉花球沾有无水硫酸铜粉末) | / |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
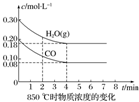 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 24g镁的最外层电子数为NA | |
| B. | 常温常压下,18g H2O含有的原子总数为3 NA | |
| C. | 标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5 NA | |
| D. | 常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H3<0 | |
| B. | 正交硫比单斜硫稳定 | |
| C. | 单斜硫转化为正交硫是吸热反应 | |
| D. | 质量相等时,单斜硫能量比正交硫能量高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13:8:29 | B. | 39:24:13 | C. | 22:11:14 | D. | 26:16:57 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++2OH-+2H++SO${\;}_{4}^{2-}$═BaSO4↓+2H2O | |
| B. | 用氯化铁溶液和沸水反应制取氢氧化铁胶体:Fe3++3H2O(沸水)═Fe(OH)3↓+3H+ | |
| C. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | 澄清石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com