
½«0£®4gNaOHŗĶ1£®06g Na2CO3»ģŗĻ²¢Åä³ÉČÜŅŗ£¬ĻņČÜŅŗÖŠµĪ¼Ó0£®1mol”¤L-1Ļ”ŃĪĖį”£ĻĀĮŠĶ¼ĻńÄÜÕżČ·±ķŹ¾¼ÓČėŃĪĖįµÄĢå»żŗĶÉś³ÉCO2µÄĪļÖŹµÄĮæµÄ¹ŲĻµµÄŹĒ
A£®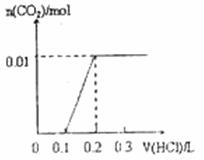 B£®
B£®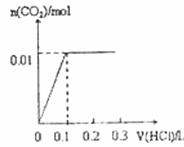
C£®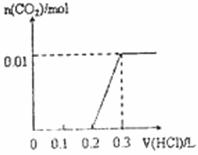 D£®
D£®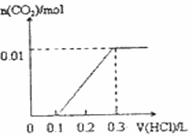
 Ęß²ŹĢāæØæŚĖćÓ¦ÓĆŅ»µćĶØĻµĮŠ“š°ø
Ęß²ŹĢāæØæŚĖćÓ¦ÓĆŅ»µćĶØĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚĻĀĆęµÄµē×Ó½į¹¹ÖŠ,µŚŅ»µēĄėÄÜ×īŠ”µÄŌ×ÓæÉÄÜŹĒ ( )
A ns2np3 B ns2np5 C ns2np4 D ns2np6
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
»ÆѧÓėÉś»īĆÜĒŠĻą¹Ų£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®ø£¶ūĀķĮÖæÉÓĆÓŚ±£“ęŗ£ĻŹ²śĘ·[ B£®¼¦µ°ĒåÖŠ¼ÓČėCuSO4ČÜŅŗ»į·¢Éś±äŠŌ
C£®ŗĻ³ÉĻš½ŗÓė¹āµ¼ĻĖĪ¬¶¼ŹōÓŚÓŠ»śøß·Ö×Ó²ÄĮĻ
D£®Ėæ³ńŗĶĆŽ»ØµÄ×é³ÉŌŖĖŲĻąĶ¬£¬·Ö×Ó½į¹¹²»Ķ¬£¬Ņņ¶ųŠŌÖŹ²»Ķ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠø÷±ķŹöÓėŹ¾ŅāĶ¼Ķ¼ÖŠŅ»ÖĀµÄŹĒ
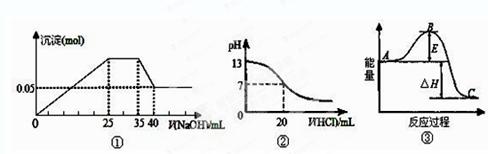
A£®Ķ¼¢Ł±ķŹ¾Ļņŗ¬M g2£«”¢Al3£«”¢NH4£«µÄŃĪČÜŅŗÖŠ
g2£«”¢Al3£«”¢NH4£«µÄŃĪČÜŅŗÖŠ µĪ¼ÓNaOHČÜŅŗŹ±£¬³ĮµķµÄĮæÓėNaOHµÄĢå»żµÄ¹ŲĻµĶ¼”£ŌņČżÖÖĄė×ÓµÄĪļÖŹµÄĮæÖ®±ČĪŖ£ŗn(Mg2£«)”Ćn(Al3£«):n( NH4£«)£½2”Ć3”Ć2
µĪ¼ÓNaOHČÜŅŗŹ±£¬³ĮµķµÄĮæÓėNaOHµÄĢå»żµÄ¹ŲĻµĶ¼”£ŌņČżÖÖĄė×ÓµÄĪļÖŹµÄĮæÖ®±ČĪŖ£ŗn(Mg2£«)”Ćn(Al3£«):n( NH4£«)£½2”Ć3”Ć2
B£®Ķ¼¢ŁÖŠŹ¹ÓƵÄNaOHµÄÅضČĪŖ10 mol/L
C£®Ķ¼¢Ś±ķŹ¾25”ꏱ£¬ ÓĆ0.1 mol”¤L£1ŃĪĖįµĪ¶Ø20 mL 0.1 mol”¤L£1 NaOHČÜŅŗ£¬ČÜŅŗµÄpHĖę¼ÓČėĖįĢå»żµÄ±ä»Æ
ÓĆ0.1 mol”¤L£1ŃĪĖįµĪ¶Ø20 mL 0.1 mol”¤L£1 NaOHČÜŅŗ£¬ČÜŅŗµÄpHĖę¼ÓČėĖįĢå»żµÄ±ä»Æ
D£®Ķ¼¢ŪÖŠĒśĻß±ķŹ¾3N2(g)+N2(g) 2NH3(g)·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»Æ£¬ČōŹ¹ÓĆ“ß»Æ¼Į£¬Bµć»įÉżøß
2NH3(g)·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»Æ£¬ČōŹ¹ÓĆ“ß»Æ¼Į£¬Bµć»įÉżøß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŹµŃé±ķĆ÷£ŗ½«ĀČĖ®µĪ¼Óµ½Ņ»ÕÅĄ¶É«ŹÆČļŹŌÖ½ÉĻ£¬ŹŌÖ½ÉĻ»į³öĻÖČēĶ¼ĖłŹ¾µÄ°ė¾¶ĀżĀżĄ©“óµÄÄŚĶāĮ½øöŌ²»·£¬ĒŅĮ½»·ŃÕÉ«²»Ķ¬£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠ²»ÕżČ·µÄŹĒ
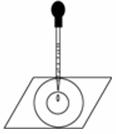
A£®“ĖŹµŃé±ķĆ÷ĀČĖ®¾ßÓŠĖįŠŌ”¢Ęư׊Ō
B£®ÄŚ»·³Ź°×É«Ķā»·³ŹŗģÉ«»ņĒ³ŗģÉ«
C£®ÄŚĶā»·ÉĻŃÕÉ«µÄ²īŅģ±ķĆ÷“Ė±ä»Æ¹ż³ĢÖŠ£¬ÖŠŗĶ·“Ó¦±ČŃõ»Æ»¹Ō·“Ó¦æģ
D£®ĀČĖ®ÖŠŠĪ³É“ĪĀČĖįµÄ·“Ó¦ÖŠ»¹Ō²śĪļŹĒHClO
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijĪŽÉ«ČÜŅŗÄÜÓėĀĮ·“Ó¦·Å³öĒāĘų£¬ŌņøĆČÜŅŗÖŠæĻ¶Ø²»ÄÜ“óĮæ¹²“ęµÄĄė×Ó×éŹĒ
A£®NH4+”¢Na£«”¢Ba2£«”¢Cl£ B£®Na£«”¢I£”¢HCO3£”¢SO42-
C£®K£«”¢Cl£”¢SO32-”¢AlO2- D£®Na£«”¢Mg2£«”¢SO42-”¢Cl£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ij»Æѧ»ī¶ÆŠ”×éÉč¼ĘČēĻĀĶ¼ĖłŹ¾£Ø²æ·Ö¼Š³Ö×°ÖĆŅŃĀŌČ„£©ŹµŃé×°ÖĆ£¬ŅŌĢ½¾æ³±ŹŖµÄCl2ÓėNa2CO3·“Ó¦µĆµ½µÄ¹ĢĢåĪļÖŹµÄ³É·Ö”£
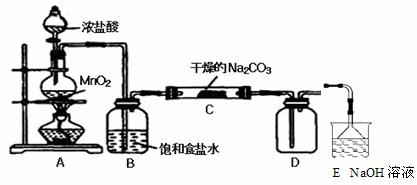
ĻņC×°ÖĆÖŠĶØČėŅ»¶ØĮæµÄĀČĘųŗ󣬲āµĆֻɜ³ÉŅ»ÖÖĘųĢåCl2O”£æÉŅŌČ·¶ØµÄŹĒCµĆµ½µÄ¹ĢĢå×ī¶ąŗ¬ÓŠČżÖÖĪļÖŹ£¬ŗ¬ÓŠĀČŌŖĖŲµÄŃĪÖ»ÓŠŅ»ÖÖ£¬ĒŅŅ»¶Øŗ¬ÓŠNaHCO3£¬ĻÖ¶ŌCÖŠµĆµ½µÄ¹ĢĢå³É·Ö½ųŠŠ²ĀĻėŗĶŃéÖ¤”£
¢ŁĢį³öŗĻĄķ²ĀĻė£ŗŅ»¶Øŗ¬ÓŠNaHCO3ŗĶ”””””””” £»æÉÄÜŗ¬ÓŠŹ£ÓąµÄNa2CO3”£
¢ŚÉč¼Ę·½°ø£¬½ųŠŠ³É·Ö¼ģŃé£ŗ
ĒėĶź³ÉŹµŃé²½Öč3”¢4ŅŌ¼°Ō¤ĘŚĻÖĻóŗĶ½įĀŪ²¢½«“š°øĢīČėĻĀ±ķµÄĻąÓ¦æÕøńÄŚ”£
ĻŽŃ”ŹµŃéŹŌ¼Į£ŗÕōĮóĖ®”¢Ļ”HNO3”¢BaCl2ČÜŅŗ”¢³ĪĒåŹÆ»ŅĖ®”¢AgNO3ČÜŅŗ”¢Ę·ŗģ”¢Ļ”ŃĪĖį
| Źµ Ńé ²½ Öč | Ō¤ ĘŚ ĻÖ Ļó ŗĶ ½į ĀŪ |
| ²½Öč1£ŗČ”CÖŠµÄÉŁĮæ¹ĢĢåѳʷӌŹŌ¹ÜÖŠ£¬¼ÓČėÕōĮóĖ®ÖĮ¹ĢĢåČܽā£¬Č»ŗóø÷Č”1”«2mLĖłµĆČÜŅŗ·Ö±šÖĆÓŚ¼×”¢ŅŅĮ½Ö§ŹŌ¹ÜÖŠ”£ | µĆµ½ĪŽÉ«ČÜŅŗ |
| ²½Öč2£ŗĻņ¼×ŹŌ¹ÜÖŠ¼ÓČė¹żĮæµÄBaCl2ČÜŅŗ£¬¾²ÖĆ”£ | ČōČÜŅŗ±ä»ė×Ē£¬Ö¤Ć÷¹ĢĢåÖŠŗ¬ÓŠ ”£ |
| ²½Öč3£ŗČ”¼×ŹŌ¹ÜÖŠÉĻ²ćĒåŅŗÉŁŠķÓŚĮķŅ»Ö»ŹŌ¹ÜÖŠ£¬µĪ¼ÓÉŁĮæ £¬³ä·ÖÕńµ“”£ | Čō £¬ Ö¤Ć÷¹ĢĢåÖŠŗ¬ÓŠNaHCO3 ”£ |
| ²½Öč4£ŗĻņŅŅŹŌ¹ÜÖŠĻČ¼ÓČė¹żĮæµÄ £¬ ŌŁµĪČėÉŁĮæ ČÜŅŗ”£ | ČōÉś³É°×É«³Įµķ£»Ö¤Ć÷¹ĢĢåÖŠŗ¬ÓŠ______”£ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¹ūÖŌŚÉś²ś¹ż³ĢÖŠĢķ¼ÓŃĒĮņĖį¼°ĘäŃĪĄą£¬ŅŌŅÖÖĘÓŠŗ¦Ī¢ÉśĪļµÄÉś³¤¼°æ¹Ńõ»Æ”£Ä³»ÆѧŠĖȤŠ”×é²éŌÄĪÄĻ×ŗó£¬ÓĆĻĀĶ¼ĖłŹ¾×°ÖĆ²ā¶Øij¹ūÖѳʷ֊SO2²ŠĮōĮ攣
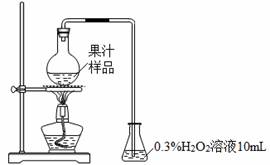
ŹµŃé²½Öč£ŗ
£Ø¢”£©ŌŚÉÕĘæÖŠ¼ÓČė50.00 mL¹ūÖѳʷÓė3mLÅØĮņĖįµÄ»ģŗĻŅŗ£¬¼ÓČČ10 min”£
£Ø¢¢£©ŅĘ³ö׶ŠĪĘ棬ŃøĖŁµĪČė2~3µĪ·ÓĢŖŹŌŅŗ£¬ÓĆ0.01000 mol”¤L£1NaOH±ź×¼ČÜŅŗµĪ¶Ø”£
»Ų“šĪŹĢā£ŗ
£Ø1£©ŹµŃéŹŅÅäÖĘNaOH±ź×¼ČÜŅŗŹ±£¬²»ŠčŅŖÓƵ½µÄŅĒĘ÷ŹĒ ”£
A£®ČŻĮæĘæ B£®½ŗĶ·µĪ¹Ü C£®ÉÕĘæ D£®²£Į§°ō
£Ø2£©½«50. 00 mL¹ūÖѳʷÓė3mLÅØĮņĖį»ģŗĻµÄ²Ł×÷ŹĒ ”£
£Ø3£©×¶ŠĪĘæÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ ”£
£Ø4£©Čō²½Öč£Ø¢¢£©ĻūŗÄNaOH±ź×¼ČÜŅŗ25. 00 mL£¬Ōņ¹ūÖѳʷ֊SO2²ŠĮōĮæŹĒ g/L”£
£Ø5£©ČōøÄÓĆ0.5%µÄµāĖ®10 mL×÷ĪüŹÕŅŗ£¬ŹµŃéÖŠĻūŗÄNaOH±ź×¼ČÜŅŗĢå»ż ”£
A£®V = 25 mL B£®25 mL£¼V£¼50 mL C£®V£¾50 mL
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
SO2”¢NOŹĒ“óĘųĪŪČ¾Īļ”£ĪüŹÕSO2 ŗĶNO£¬»ńµĆNa2S2O4ŗĶNH4NO3²śĘ·µÄĮ÷³ĢĶ¼ČēĻĀ£ØCeĪŖīęŌŖĖŲ£©£ŗ
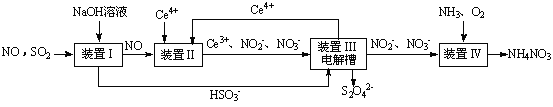
£Ø1£©×°ÖĆ¢ńÖŠÉś³ÉHSO3£µÄĄė×Ó·½³ĢĪŖ ”£
£Ø2£©ŗ¬Įņø÷Ī¢Į££ØH2SO3”¢HSO3£ŗĶSO32££©“ęŌŚÓŚSO2ÓėNaOHČÜŅŗ·“Ó¦ŗóµÄČÜŅŗÖŠ£¬ĖüĆĒµÄĪļÖŹµÄĮæ·ÖŹżX(i)ÓėČÜŅŗpH µÄ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£
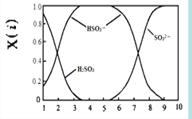
¢ŁĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £ØĢī×ÖÄøŠņŗÅ£©”£
a£®pH=8Ź±£¬ČÜŅŗÖŠc(HSO3£) < c(SO32£)
b£®pH=7Ź±£¬ČÜŅŗÖŠc(Na+) =c(HSO3£)+c(SO32£)
c£®ĪŖ»ńµĆ¾”æÉÄÜ“æµÄNaHSO3£¬æɽ«ČÜŅŗµÄpHæŲÖĘŌŚ4”«5×óÓŅ
¢ŚĻņpH=5µÄNaHSO3ČÜŅŗÖŠµĪ¼ÓŅ»¶ØÅØ¶ČµÄCaCl2ČÜŅŗ£¬ČÜŅŗÖŠ³öĻÖ»ė×Ē£¬pH½µĪŖ2£¬ÓĆ»ÆŃ§Ę½ŗāŅʶÆŌĄķ½āŹĶČÜŅŗpH½µµĶµÄŌŅņ£ŗ ”£
£Ø3£©×°ÖĆ¢ņÖŠ£¬ĖįŠŌĢõ¼žĻĀ£¬NO±»Ce4+Ńõ»ÆµÄ²śĪļÖ÷ŅŖŹĒNO3£”¢NO2££¬Š“³öÉś³ÉNO3£µÄĄė×Ó·½³ĢŹ½ ”£
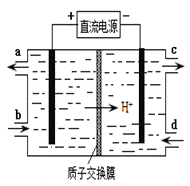
£Ø4£©×°ÖĆ¢óµÄ×÷ÓĆÖ®Ņ»ŹĒŌŁÉśCe4+£¬ĘäŌĄķČēĻĀĶ¼ĖłŹ¾”£
¢ŁÉś³ÉCe4+µÄµē¼«·“Ó¦Ź½ĪŖ ”£
¢ŚÉś³ÉCe4+“Óµē½ā²ŪµÄ £ØĢī×ÖÄøŠņŗÅ£©æŚĮ÷³ö”£
£Ø5£©ŅŃÖŖ½ųČė×°ÖĆ¢ōµÄČÜŅŗÖŠ£¬NO2£µÄÅضČĪŖa g·L-1£¬ŅŖŹ¹1 m3øĆČÜŅŗÖŠµÄNO2£ĶźČ«×Ŗ»ÆĪŖNH4NO3£¬ŠčÖĮÉŁĻņ×°ÖĆ¢ōÖŠĶØČė±ź×¼×“æöĻĀµÄO2 L”££ØÓĆŗ¬a“śŹżŹ½±ķŹ¾£¬¼ĘĖć½į¹ū±£ĮōÕūŹż£©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com