
【题目】某芳香烃的分子式为C8H10,其一溴代物的同分异构体有
A. 14种 B. 9种 C. 5种 D. 12种
科目:高中化学 来源: 题型:
【题目】某市中考化学实验操作考试有四个考题:①蒸馏;②H2的化学性质;③二氧化碳的制取、收集和验满;④氧气的制取、收集和验满。考试的方法是由考生抽签确定考题,小凯同学抽签后被监考老师引导至准备了下列仪器和药品的实验台前:

请回答:
(1)指出上图中仪器a的名称:_______;
(2)由实验台上提供的仪器和药品,你认为小凯抽到的是第____个考题;
(3)以下是小凯完成该实验主要操作过程的示意图。按评分标准,每项操作正确得1分,满分5分,实验完毕后小凯得了3分。请找出他失分的操作并说明原因:______________________、______________________;
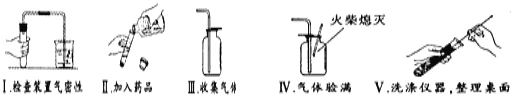
(4)仅用上述仪器(药品另选),也能完成另一种常见气体的实验室制取,化学方程式为:______________;若增加________ (填一种玻璃仪器名称)还能组装成高锰酸钾制氧气的发生装置。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化石墨烯具有优良的生物亲和性和亲水性,可通过下列实验方法制得(装置如图所示):
①低温阶段:控温0℃,烧瓶中加入3g石墨烯、12 g KMnO4和100 mL浓硫酸,搅拌反应20 min;
②中温阶段:水浴控温15℃,反应2 h;再控湿35℃,反应40 min;
③高温阶段:用220 mL高纯水稀释反应液,控温80℃,反应20 min,再滴入10 mL 30%H2O2溶液,控温45℃,待胶体变为金黄色,静置24 h;倾出上层清液,用盐酸洗涤下层沉淀,过滤、高纯水洗涤、真空干燥,得到氧化石墨烯。
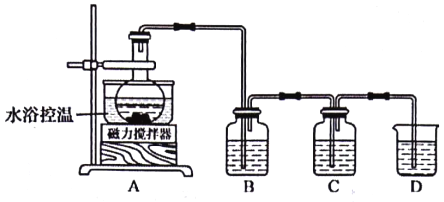
回答下列问题:
(1)将石墨中的层状结构剥离就能得到石墨烯,石墨烯的化学成分是_______(写名称)。
(2)“低温阶段”控温0℃的方法是____________。
(3)装置B装入酸性KMnO4溶液,其目的是_________;装置C用于检测CO2的生成,则判断有CO2生成的实验现象是_______________。
(4)“高温阶段”中,控温80℃之前,必须加入高纯水稀释反应液,稀释的操作方法是_______。“高温阶段”若温度过高,反应液极易发生“暴沸”而导致实验失败,其原因是__________。
(5)“高温阶段”滴入10 mL 30% H2O2溶液的目的是为了除去过量的KMnO4,反应的化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳的氧化物对环境的影响较大,CO是燃煤工业生产中的大气污染物,CO2则促进了地球的温室效应。给地球生命带来了极大的威胁。
(1)已知:①甲醇的燃烧热△H=-726.4kJ·mol-1
②H2(g)+ ![]() O2(g)=H2O(l) △H=-285.8kJ·mol-1。
O2(g)=H2O(l) △H=-285.8kJ·mol-1。
则二氧化碳和氢气合成液态甲醇,生成液态水的热化学方程式为_____________________________。
(2)二氧化碳合成CH3OH 的热化学方程式为CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H1,过程中会产生副反应:CO2(g)+H2(g)
CH3OH(g)+H2O(g)△H1,过程中会产生副反应:CO2(g)+H2(g)![]() CO(g)+H2O(g)△H2。图1是合成甲醇反应中温度对CH3OH、CO的产率影响曲线图,△H2________0(填“>”或“<”)。增大反应体系的压强,合成甲醇的反应速率___________(填“增大”“减小”或“ 不变”),副反应的化学平衡________(填“向正反应方向”“向逆反应方向”或“不”)移动。
CO(g)+H2O(g)△H2。图1是合成甲醇反应中温度对CH3OH、CO的产率影响曲线图,△H2________0(填“>”或“<”)。增大反应体系的压强,合成甲醇的反应速率___________(填“增大”“减小”或“ 不变”),副反应的化学平衡________(填“向正反应方向”“向逆反应方向”或“不”)移动。
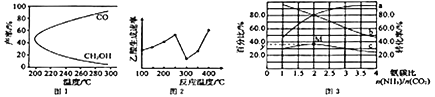
(3)以某些过渡金属氧化物作催化剂,二氧化碳与甲烷可转化为乙酸:CO2(g) +CH4(g)![]() CH3COOH(g) △H=+36.0kJ·mol-1。不同温度下,乙酸的生成速率变化曲线如图2。结合反应速率,使用催化剂的最佳温度是________℃,欲提高CH4的转化率,请提供一种可行的措施:____________________________。
CH3COOH(g) △H=+36.0kJ·mol-1。不同温度下,乙酸的生成速率变化曲线如图2。结合反应速率,使用催化剂的最佳温度是________℃,欲提高CH4的转化率,请提供一种可行的措施:____________________________。
(4)一定条件下,CO2 与NH3 可合成尿素[CO(NH2)2]:CO2(g)+2NH3(g)![]() CO(NH2)2(g)+H2O(g)△H。某温度下。在容积为1L的恒容密闭容器中,加入一定氨碳比
CO(NH2)2(g)+H2O(g)△H。某温度下。在容积为1L的恒容密闭容器中,加入一定氨碳比![]() 的3molCO2 和NH3的混合气体。图3是有关量的变化曲线,其中表示NH3转化率的是曲线________(填“a”或“b”),曲线c 表示尿素在平衡体系中的体积分数变化曲线,则M点的平衡常数K=________,y=________。
的3molCO2 和NH3的混合气体。图3是有关量的变化曲线,其中表示NH3转化率的是曲线________(填“a”或“b”),曲线c 表示尿素在平衡体系中的体积分数变化曲线,则M点的平衡常数K=________,y=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
A. 0.1 mol CH4分子所含质子数为1.6 NA
B. 在0℃,101kPa时,22.4 L H2中含有NA个氢原子
C. 16 g氧气和16 g臭氧所含的原子数均为NA
D. NA个CO分子和11.2L CH4的质量比为7:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.在一定温度下将2molA和2molB两种气体混合于2L密闭容器中,发生如下反应:3A(g)+B(g)=- 2C(g)+ 2D(g),2 分钟末反应达到平衡状态,生成了0.6mol D,回答下列问题:
(1)用D表示2min内的平均反应速率为____________,A的转化率为_____________。
(2)如果缩小容器容积(温度不变),则平衡体系中混合气体的密度_________(填“增大”、“减少”或“不变”)。
(3)若开始时只加C和D各4/3mol,要使平衡时各物质的质量分数与原平衡相等,则还应加入_____________mol B 物质。
(4)若向原平衡体系中再投入1molA和1molB,B的转化率_________(填“增大”、“减少”或“不变”)。
II.有人设计出利用CH3OH 和O2的反应,用铂电极在KOH 溶液中构成原电池。电池的总反应类似于CH3OH 在O2中燃烧,则:
(1)每消耗1molCH3OH 可以向外电路提供___________mole-;
(2)负极电极反应式为________________________。
(3)电池放电后,溶液的pH_________(填“增大”、“减少”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳跟浓硫酸共热产生的混合气体X和铜跟浓硝酸反应产生的混合气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
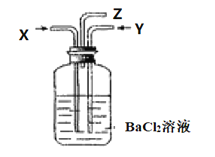
A. 洗气瓶中产生的沉淀是BaCO3
B. 在Z导管出来的气体中无CO2
C. 洗气瓶中产生的沉淀是BaSO3
D. 在Z导管口有红棕色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2(g)+O2(g)![]() 2SO3(g)从正方向开始,并达到了平衡,此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是
2SO3(g)从正方向开始,并达到了平衡,此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是
A. 新平衡体系中,SO2和O2物质的量之比仍为2∶1
B. 平衡向正反应方向移动,原因是正反应速率增大,逆反应速率减小
C. 新平衡体系与旧平衡体系比较,SO3的浓度肯定增大
D. 若采取的措施是缩小容器的容积,则新旧平衡中SO2和O2的转化率之比都是1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验事实,不能得到相应结论的是
选项 | 实验操作和现象 | 结论 |
A | 向醋酸溶液中滴加少量Na2SiO3溶液,观察到白色沉淀 | 醋酸的酸性强于H2SiO3 |
B | 向均盛有2mL5% H2O2溶液的两支试管中分别滴入0.2mol/LFeCl3和0.3mol/LCuCl2溶液各1mL,前者生成气泡的速率更快 | 催化效果: Fe3+> Cu2+ |
C | 向一定浓度的醋酸溶液中加入镁条,产生气泡的速率会先加快再减慢 | 反应产生气泡速度变化,是因为醋酸电离平衡先正向移动,再逆向移动 |
D | 常温下分别测等浓度的醋酸和氨水pH,二者的pH 分别为2和12 | 常温下,醋酸和氨水的电离平衡常数相等 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com