
| A. | 1摩尔任何气体都含有6.02×1023个分子 | |
| B. | 0.012Kg12C中含有6.02×1023个碳原子 | |
| C. | 1摩尔水中含有2mol氢和1mol氧 | |
| D. | 1molH2O中含有3 mol原子 |
分析 A.1mol任何物质都约含有6.02×1023个微粒,构成物质的微粒有分子、原子和离子;
B.0.012kg碳原子的物质的量为:$\frac{12g}{12g/mol}$=1mol;
C.使用物质的量应指明具体的物质或微粒;
D.1molH2O中含有2molH和1molO.
解答 解:A.1mol任何物质都约含有6.02×1023个微粒,1摩尔任何气体都含有6.02×1023个分子,故A正确;
B.0.012kg12C中所含微粒数为阿伏伽德罗常数,0.012kg碳原子(12C)的物质的量为1mol,所含有的碳原子数为NA个,约含有6.02×1023个12C,故B正确;
C.2mol氢和1mol氧指代不明,不能确定原子还是分子,1mol水分子中含有2mol氢原子和1mol氧原子,故C错误;
D.1molH2O中含有2molH和1molO,1molH2O中含有3 mol原子,故D正确.
故选C.
点评 本题考查物质的量、微粒数目计算等,比较基础,注意使用物质的量时应指明具体的物质或微粒,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1,3-二甲基戊烷 | B. | 2-甲基-3-乙基丁烷 | ||
| C. | 3,4-二甲基戊烷 | D. | 2,3-二甲基戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 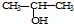 将与浓硫酸共热制备CH3-CH═CH2 将与浓硫酸共热制备CH3-CH═CH2 | |
| B. | 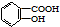 与适量NaHCO3溶液反应制备 与适量NaHCO3溶液反应制备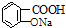 | |
| C. | 检验蔗糖水解产物是否具有还原性,可向水解后的溶液中直接加入新制的Cu(OH)2悬浊液并加热 | |
| D. | 用溴水即可检验CH2=CH-CHO中的碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在离子化合物里,只存在离子键 | |
| B. | 在共价化合物里,一定不存在离子键 | |
| C. | 非金属元素之间只能形成共价键 | |
| D. | 由不同种元素组成的多原子分子里,一定只存在极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2+、K+、SO42-、OH- | B. | Na+、Ag+、NO3-、Cl- | ||
| C. | H+、Ba2+、NO3-、Cl- | D. | Ca2+、K+、CO32-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com