

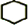
 ,B名称是1,2-二溴环己烷
,B名称是1,2-二溴环己烷 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$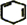 +2NaBr+2H2O.
+2NaBr+2H2O. 分析 由合成路线可知,反应①为光照条件下的取代反应,所以A为 ,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为
,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为 ,反应④为卤代烃的消去反应,生成环己二烯,结合物质的性质及化学用语来解答.
,反应④为卤代烃的消去反应,生成环己二烯,结合物质的性质及化学用语来解答.
解答 解:由合成路线可知,反应①为光照条件下的取代反应,所以A为 ,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为
,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为 ,反应④为卤代烃的消去反应,生成环己二烯,
,反应④为卤代烃的消去反应,生成环己二烯,
(1)由上述分析可知,A为 ,B为
,B为 ,名称为1,2-二溴环己烷,故答案为:
,名称为1,2-二溴环己烷,故答案为: ;1,2-二溴环己烷;
;1,2-二溴环己烷;
(2)反应①为取代反应,③为加成反应,故答案为:取代反应;加成反应;
(3)反应④的化学方程式为 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O,故答案为:
+2NaBr+2H2O,故答案为: +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O.
+2NaBr+2H2O.
点评 本题考查有机物的合成,为高频考点,明确反应条件与反应类型的关系来推出各物质是解答本题的关键,题目难度不大,注意卤代烃的水解、消去反应的条件,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 四种元素A、B、C、D分别为O、Ca、Na、Ar | |
| B. | 元素A、B、C两两组成的化合物可为CaO、CaO2、Na2O、Na2O2等 | |
| C. | 元素A、C简单离子的半径大小关系为A<C | |
| D. | 元素B、C的单质与水都能剧烈反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
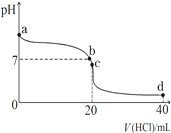 (1)明矾可用于净水,用离子方程式解释其原因Al3++3H2O?Al(OH)3(胶体)+3H+.把FeCl3溶液蒸干、灼烧、最后得到的主要固体产物是Fe2O3.
(1)明矾可用于净水,用离子方程式解释其原因Al3++3H2O?Al(OH)3(胶体)+3H+.把FeCl3溶液蒸干、灼烧、最后得到的主要固体产物是Fe2O3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
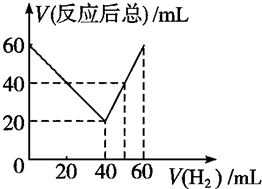 某气态不饱和链烃CnHm在一定条件下与H2加成为CnHm+x,取CnHm和H2混合气体共60mL进行实验,发现随混合气中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温同压下测定).由此可知x的数值为( )
某气态不饱和链烃CnHm在一定条件下与H2加成为CnHm+x,取CnHm和H2混合气体共60mL进行实验,发现随混合气中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温同压下测定).由此可知x的数值为( )| A. | 4 | B. | 3 | C. | 2 | D. | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧杯①中,若构成微型电池,负极反应式为2Al-6e-=2Al3+,正极反应式为 6H++6e-=3H2↑ | |
| B. | 烧杯①中,若将电解质溶液换成浓硝酸,构成微型电池时铝为负极,铜为正极 | |
| C. | 烧杯②中,若铁、铜构成微型电池,则铁为负极;若铝、铁构成微型电池,则铁为正极 | |
| D. | 烧杯②中,固体最终完全溶解,溶液呈蓝色.向溶液中滴加KSCN溶液,溶液不变色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时负极反应为:Zn-2e-+2OH--Zn(OH)2 | |
| B. | 放电时正极发生氧化反应 | |
| C. | 放电时每转移2mol电子,反应的锌的质量是65g | |
| D. | 放电时化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ | |
| B. | HS-水解的离子方程式:HS-+H2O?S2-+H3O+ | |
| C. | CO32-水解的离子方程式:CO32-+2 H2O?H2CO3+2OH- | |
| D. | 用FeS为沉淀剂除去废水中的Hg2+:FeS(s)+Hg2+(aq)=HgS(s)+Fe2+(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
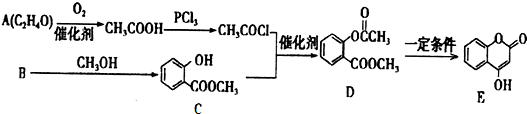
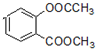 +3NaOH→CH3COONa+CH3OH+
+3NaOH→CH3COONa+CH3OH+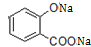 +H2O.
+H2O.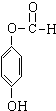
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com