
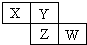
 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法不正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法不正确的是( )| A、氢化物的稳定性:X>Y |
| B、W的最高价氧化物对应水化物的酸性比Z的强 |
| C、Y的非金属性比X的强 |
| D、Y与Z形成的化合物是形成酸雨的主要物质 |


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | |||||||||||||||||
| D | E | G | |||||||||||||||
| J | L | ||||||||||||||||
| M | Q | ||||||||||||||||
| 化学键 | G-J | J-J | G=G |
| 键能/(KJ?mol-1) | 460 | 176 | 497 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.204×1024 |
| B、1.204×1023 |
| C、2.408×1024 |
| D、2.408×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 |
| B、向0.1mol?L-1的FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具有漂白性 |
| C、将碘水倒入分液漏斗中,加入适量乙醇,振荡后静置,可降碘萃取到乙醇中 |
| D、向锌粒与稀H2SO4的反应溶液中加入CuSO4,产生气泡的速度加快,说明CuSO4对此反应有催化作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
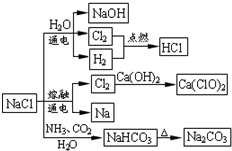 NaCl是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( )
NaCl是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( )| A、常温下干燥Cl2能用钢瓶贮运,所以Cl2与铁不反应 |
| B、25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| C、源石灰乳与Cl2的反应中Cl2既是氧化剂,又是还原剂 |
| D、图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com