
镀镍废水中含有氰根(CN-),其质量浓度往往高于国家排放标准规定的范围,需要进行破氰处理。用化学法处理电镀废水中的氰化物,一般采用碱性氰化法和双氧水氧化法。
I、碱性氯化法是在废水中加入NaOH使Ni2+生成Ni(OH)2沉淀,同时加NaClO将CN-氧化为无毒物质,但此法中ClO-在碱性条件下会和Ni2+反应生Ni(OH)3沉淀和Cl-而大量消耗,反应的离子反应方程式为_______________________________________;
Ⅱ、双氧水氧化法的简易工艺流程如下:
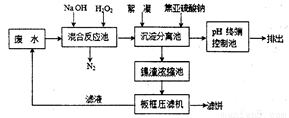
(1)混合反应池中,在碱性条件下H2O2氧化CN-却不会和Ni2+反应,此反应的离子方程式为______________;H2O2还会以质量比为25:2的比例氧化废水中的有机添加剂,降低废水的COD值。
(2)沉淀分离池中,加入焦亚硫酸钠(Na2S2O5)还原除去过量的H2O2,否则会影响沉淀的絮凝沉降,请分析原因________________________________;
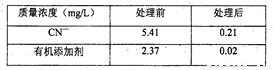
(3)向废水中加入30%H2O2(密度为1.11g/mL)的用量为1mL/L,处理前后CN-和有机添加剂的质量浓度如下表所示,若不考虑H2O2的自身分解和溶液体积的变化。请计算需在沉淀分离池中至少加入焦亚硫 酸钠(Na2S2O5)的量为_________g/L(计算结果保留到小数点后两位)。写出计算过程。
科目:高中化学 来源:2015-2016学年浙江省宁波市高二下学期期中考试化学试卷(解析版) 题型:选择题
物质的鉴别有多种方法。下列能达到鉴别目的的是
① 用水鉴别苯、乙醇、溴苯 ② 用相互滴加的方法鉴别Ca(OH)2和NaHCO3溶液③ 点燃鉴别甲烷和乙炔
A.① ② B.①③ C.②③ D.①②③
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三下第七次月考理综化学试卷(解析版) 题型:推断题
某有机物A(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多,是一种常用的食品添加剂。该化合物具有如下性质:
①在25℃时,A的电离平衡常数K1=3.9×10-4,K2=5.5×10-6
②A + RCOOH(或ROH) 有香味的产物
有香味的产物
③1 mol A 慢慢产生1.5 mol气体
慢慢产生1.5 mol气体
④核磁共振氢谱表明A分子中有5种不同化学环境的氢原子,与A相关的反应框图如下:
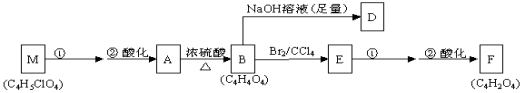
(1)根据化合物A的性质,对A的结构可作出的判断是_______。
(a)肯定有碳碳双键 (b)有两个羧基
(c)肯定有羟基 (d)有-COOR官能团
(2)写出A、D、F、M的结构简式:A:_________________;D:__________________;
F:_________________;M:__________________。
(3)写出A→B、B→E的反应类型:A→B______________; B→E_______________。
(4)写出M→A的第①步反应的反应条件:_______________________;
写出E→F的第①步反应的反应方程式: ___________________________________。
(5)在催化剂作用下,B与乙二醇可发生缩聚反应,生成的高分子化合物用于制造玻璃钢。写出该反应的化学方程式:__________________________________________。
(6)写出一种与A具有相同官能团的A的同分异构体的结构简式________________。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁师大附中高三下学期精品考试理综化学试卷(解析版) 题型:填空题
科学研究表明,当前应用最广泛的化石燃料到本世纪中叶将枯竭,解决此危机的唯一途径是实现燃料和燃烧产物之间的良性循环:
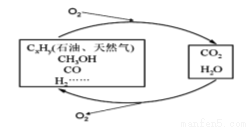
(1)一种常用的方法是在230℃、有催化剂条件下将CO2和H2转化为甲醇蒸汽和水蒸气 。下图是生成1molCH3OH时的能量变化
。下图是生成1molCH3OH时的能量变化 示意图。
示意图。
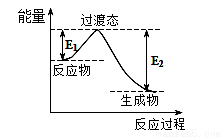
已知破坏1mol不同共价键的能量(kJ)分别是:
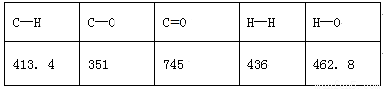
已知E1=8.2 kJ·mol-1,则E2=__________kJ·mol-1。
(2)将不同量的CO(g)和H2O(g)分别通入 到体积为2L的恒容密闭容器中进行如下反应:
到体积为2L的恒容密闭容器中进行如下反应:
CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
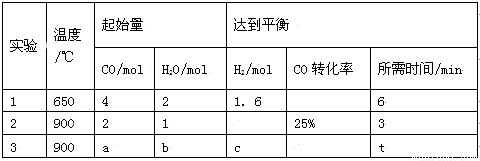
① 该反应的ΔH__________0(填“<” 或“>” )。
② 实验2条件下的平衡常数K= 。
③ 实验3中,若平衡时H2O的转化率为25%,则a/b=______。
④ 实验4,若900℃时,在容器中加入CO、H2O、CO2、H2各1mol,则此时V正 V逆(填“<” 或“>” 或“=”)。
(3)捕捉CO2可以利用Na2CO3溶液。先用Na2CO3溶液吸收CO2生成NaHCO3,然后使NaHCO3分解,Na2CO3可以进行循环使用。将100mL 0.1mol/LNa2CO3的溶液中通入112mL(已换算为标准状况)的CO2,溶液中没有晶体析出,则:
①反应后溶液中的各离子浓度由大到小的顺序是___________________________。
②反应后的溶液可以作“缓冲液” (当往溶液中加入一定量的酸和碱时,有阻碍溶液pH变化的作用),请解释其原理_____________________________________。
(当往溶液中加入一定量的酸和碱时,有阻碍溶液pH变化的作用),请解释其原理_____________________________________。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁师大附中高三下学期精品考试理综化学试卷(解析版) 题型:选择题
分子式为C5H10O3的有机物与NaHCO3溶液反应时,生成C5H9O3Na;而与金属钠反应时生成C5H8O3N a2。则该有机物的同分异构体的种类(不考虑立体异构)有
a2。则该有机物的同分异构体的种类(不考虑立体异构)有
A.10种 B.11种 C.12种 D.13种
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前热身(五模)化学试卷(解析版) 题型:选择题
下列物质的转化在给定条件下不能实现的是
A.Ca(ClO)2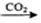 (aq)HClO(aq)
(aq)HClO(aq) HCl(aq)
HCl(aq)
B.H2SiO3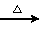 SiO2
SiO2 SiCl4
SiCl4
C.Al2O3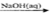 NaAlO2
NaAlO2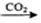 Al(OH)3
Al(OH)3
D.Fe2O3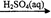 Fe2(SO4)3(aq)
Fe2(SO4)3(aq) 无水Fe2(SO4)3
无水Fe2(SO4)3
查看答案和解析>>
科目:高中化学 来源:2016届海南师大附中高三临考模拟化学试卷(解析版) 题型:选择题
科学家预言,燃料电池将是 21 世纪获得电能的重要途径。近几年开发的甲醇燃料电池是采用铂作电极催化剂,工作原理是将电极插入KOH溶液中,然后在两极分别添加甲醇和氧气,若a极上添加甲醇; b极:2H2O+O2+4e-=4OH-。 关于此燃料电池的下列说法中错误的是( )
A.a极为负极,b极为正极。
B.放电过程中,a、b电极上均发生氧化还原反应。
C.该电池工作时添加甲醇的一极,附近溶液的 pH 降低,反应的离子方程式为:CH3OH+8OH-―6e-=CO32-+6H2O
D.若用此电源电解饱和食盐水,每消耗0.1molO2则阴极理论上生成0.2molCl2。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁沈阳二中高一6月月考化学试卷(解析版) 题型:简答题
为治理环境,减少雾霾,应采取措施减少二氧化硫、氮氧化物(NOx)和CO2的排放量。
Ⅰ.处理NOx的一种方法是利用甲烷催化还原NOx。
①CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ· mol-1
4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ· mol-1
②CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH2=-586.7 kJ· mol-1
N2(g)+CO2(g)+2H2O(g) ΔH2=-586.7 kJ· mol-1
(1)若用4.48 L CH4还原NO生成N2,则放出的热量为 kJ(保留两位小数)。(气体体积已折算为标准状况下)
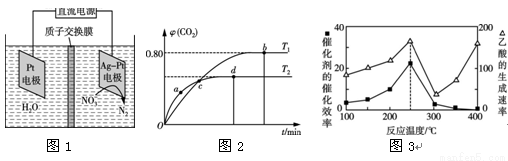
(2)用电化学处理含NO3—的废水,电解的原理如图1所示,则电解时阴极的电极反应式为 ;
Ⅱ.利用I2O5消除CO污染的反应为5CO(g)+I2O5(s) 5CO2(g)+I2(s)。不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入4 mol CO,测得CO2的体积分数(φ)随时间(t)变化曲线如图2所示。
5CO2(g)+I2(s)。不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入4 mol CO,测得CO2的体积分数(φ)随时间(t)变化曲线如图2所示。
(3)T1时,该反应的化学平衡常数的数值为 。
(4)下列说法不正确的是 (填字母)。
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,在原容器中充入一定量氦气,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb<Kd
Ⅲ.以二氧化钛表面覆盖Cu2Al2O4 为催化剂,可以将CO2和CH4通过反应CO2(g)+CH4(g) CH3COOH(g) ΔH<0直接转化成乙酸。在不同温度下
CH3COOH(g) ΔH<0直接转化成乙酸。在不同温度下 催化剂的催化效率与乙酸的生成速率如图3所示。
催化剂的催化效率与乙酸的生成速率如图3所示。
(5)250~300 ℃时,乙酸的生成速率减小的主要原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com