
| A. | 戊烷与乙烷 | B. | 淀粉和纤维素 | C. | 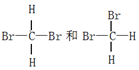 | D. | CH3CH2CH2CH3和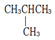 |
科目:高中化学 来源: 题型:选择题
| A. | 1 mol KClO3所具有的总能量高于1 mol KCl所具有的总能量 | |
| B. | KClO3分解速率快慢主要取决于反应① | |
| C. | 1 g KClO3,1 g MnO2,0.1 g Mn2O7混合加热,充分反应后MnO2质量为1 g | |
| D. | 将固体二氧化锰碾碎,可加快KClO3的分解速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
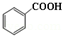 +C2H5OH$\stackrel{H_{2}SO_{4}}{?}$
+C2H5OH$\stackrel{H_{2}SO_{4}}{?}$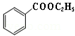 +H2O
+H2O| 沸点(℃) | 密度(g•cm-3) | |
| 苯甲酸 | 249 | 1.2659 |
| 苯甲酸乙酯 | 212.6 | 1.05 |
| 乙醇 | 78.5 | 0.7893 |
| 环已烷 | 80.8 | 0.7785 |
| 乙醚 | 34.51 | 0.7318 |
| 环已烷、乙醇和水共沸物 | 62.1 |
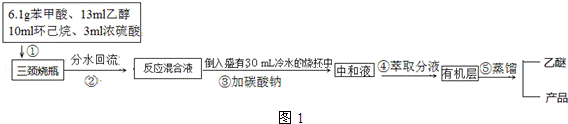
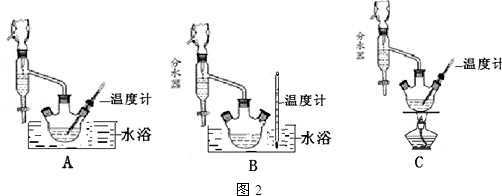
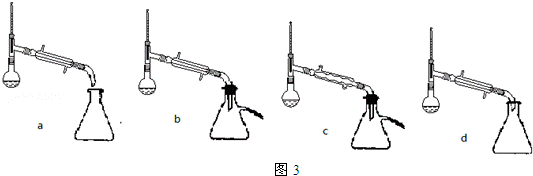
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化钠水解:S2-+2H2O?H2S↑+2OH- | |
| B. | 硫氢化钠水解:HS-+H2O?H3O++S2- | |
| C. | 硫化钾水解:S2-+H2O?HS-+OH- | |
| D. | 硫酸铝溶液跟碳酸氢钠溶液反应:Al3++3HCO3-+6H2O?Al(OH)3↓+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 产物不稳定,受热即脱水而生成不饱和醛.
产物不稳定,受热即脱水而生成不饱和醛.
 ;F
;F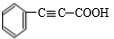 .
. +CH3CHO$\stackrel{△}{→}$
+CH3CHO$\stackrel{△}{→}$ +H2OE→F
+H2OE→F +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$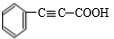 +2NaBr+2H2O
+2NaBr+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含0.1mol•L -1CaCl2的溶液:SO42-、Na+、NO 3-、Cl- | |
| B. | 使酚酞变红色的溶液:NH 4+、K+、SO42-、NO 3- | |
| C. | 澄清透明溶液:Mg 2+、Na+、Cl-、SO4 2- | |
| D. | 在含有大量HCO 3-的溶液中:Na +、NO 3-、Cl-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属原子失电子越多,其还原性越强 | |
| B. | 制成0.5L 1mol/L的Na2CO3溶液,需要Na2CO3•10H2O晶体质量为143克 | |
| C. | 相同条件下,NA个氧气分子和NA个氮气分子的密度比等于7:8 | |
| D. | 配制480 mL溶液时,选择规格为480 mL的容量瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
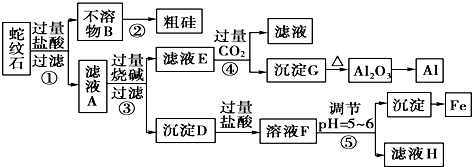
| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com