
高铁的快速发展方便了人们的出行。工业上利用铝热反应焊接钢轨间的缝隙,反应方程式如下:
2Al+Fe2O3 2Fe+Al2O3,其中Fe2O3是
2Fe+Al2O3,其中Fe2O3是
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
一定条件下,NO2跟NH3可以发生反应生成N2和H2O,反应方程式为6NO2+8NH3=7N2+12H2O。请回答:
(1)标明电子转移的方向和数目;
(2)氧化产物与还原产物的质量比是 ;
(3)若经氧化得到的N2比经还原得到的N2多2.8g,求参加反应的NO2 和NH3的质量各是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
在一容积可变的密闭容器中,aA(气)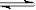 bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
A.平衡向正反应方向移动了 B.物质A的转化率减少了
C.物质B的质量分数减小了 D.化学计量数关系a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
已知NaNO2的化学式量为69,则500mL1.0 mol·L-1NaNO2溶液含有溶质质量为
A.13.8g B.69g C. 34.5g D.138g
查看答案和解析>>
科目:高中化学 来源: 题型:
现有三组实验:① 除去混在植物油中的水 ② 回收碘的CCl4溶液中的CCl4 ③ 用食用酒精浸泡中草药提取其中的有效成份。分离以上各混合液的正确方法依次是
A.分液.萃取.蒸馏 B.萃取.蒸馏.分液
C.分液.蒸馏.萃取 D.蒸馏.萃取.分液
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题
(1)根据计算用托盘天平需称取氯化钠 g。
(2)配制时,必须用到的玻璃仪器有烧杯 玻璃棒 与
(3)配制溶液有下列几步操作:a.溶解,b.摇匀,c.洗涤,d.冷却,e.称量,
f.将溶液移至容量瓶,g.贴标签,h.定容。
则正确的操作顺序是 。
(4)下列操作结果使溶液物质的量浓度偏低的是
A.没有将洗涤液转入容量瓶中, B.容量瓶洗涤后,未经干燥处理,
C.定容时,俯视容量瓶的刻度线, D.加水定容时,水的量超过了刻度线。
(5)取出该NaCl溶液10mL加水稀释到100mL,稀释后溶液中NaCl的
物质的量浓度是 。
(6)写出检验NaCl溶液中含有氯离子的有关反应方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
为证明Fe3+具有较强的氧化性,
甲同学做了如下实验:将Cu片放入Fe(NO3)3溶液中,观察到Cu片逐渐溶解,溶液由黄色变为蓝绿色,由此甲同学得到Fe3+具有较强氧化性的结论。
乙同学提出了不同的看法:“Fe(NO3)3溶液具有酸性,在此酸性条件下NO3-也能氧化Cu”,并设计实验进行探究。
已知:
| 水解反应 | 平衡常数(K) |
| Fe3+ + 3H2O | 7.9 × 10-4 |
| Fe2+ + 2H2O | 3.2 × 10-10 |
| Cu2+ + 2H2O | 3.2 × 10-7 |
请回答:
(1)稀硝酸和Cu反应的化学方程式为 。
(2)请利用所提供的试剂,帮助乙同学完成实验方案设计。
试剂:0.5mol/L Fe(NO3)3溶液、Cu片、精密pH试纸(0.5~5.0)、稀硝酸
方案:
。
(3)丙同学分别实施了甲、乙两位同学的实验方案,并在实验过程中用pH计监测溶液pH的变化,实验记录如下。
| 实验内容 | 实验现象 |
| 甲同学的实验方案 | 溶液逐渐变成蓝绿色, pH略有上升 |
| 乙同学的实验方案 | 无明显现象,pH没有明显变化。 |
①根据实验现象写出发生反应的离子方程式: 。
②导致实验过程中溶液pH略有上升的可能原因是
。
(4)请你设计更简便可行的实验方案,帮助甲同学达到实验目的:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式正确的是( )
|
| A. | H2SO4=2H++S6++4O2﹣ | B. | H2CO3=2H++CO32﹣ |
|
| C. | Ba(OH)2=Ba2++2OH﹣ | D. | Na2CO3=Na2++CO32﹣ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com