
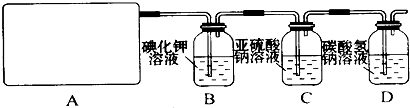
| A£® | ŅŅĖįÓėŅŅĖįŅŅõ„ | B£® | äå±½ÓėĖ® | C£® | ¾Ę¾«ÓėĖ® | D£® | ±½ÓėCCl4 |
·ÖĪö »„²»ĻąČܵÄŅŗĢåæɲÉÓĆ·ÖŅŗ·½·Ø·ÖĄė£¬»„ČܵÄŅŗĢå²ÉÓĆÕōĮó·½·Ø·ÖĄė£¬Ń”ĻīÖŠ»ģŗĻĪļæÉŅŌÓĆ·ÖŅŗĀ©¶··ÖĄėĖµĆ÷øĆ»ģŗĻĪļÖŠĮ½ÖÖĪļÖŹ²»»„ČÜ£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗA£®ŅŅĖįŅŅõ„ŗĶŅŅĖį»„ČÜ£¬Ó¦øĆ²ÉÓĆÕōĮó·½·Ø·ÖĄė£¬¹ŹA“ķĪó£»
B£®äå±½ŗĶĖ®²»»„ČÜ£¬¶žÕß»ģŗĻŹ±·Ö²ć£¬ĖłŅŌæÉŅŌ²ÉÓĆ·ÖŅŗ·½·Ø·ÖĄė£¬¹ŹBÕżČ·£»
C£®ŅŅ“¼ŗĶĖ®»„ČÜ£¬Ó¦øĆ²ÉÓĆÕōĮó·½·Ø·ÖĄė£¬¹ŹC“ķĪó£»
D£®±½ŗĶĖÄĀČ»ÆĢ¼»„ČÜ£¬ĖłŅŌÓ¦øĆ²ÉÓĆÕōĮó·½·Ø·ÖĄė£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ·ÖĄėŗĶĢį“棬Ć÷Č·ĪļÖŹŠŌÖŹÓė·ÖĄė·½·ØµÄ¹ŲĻµŹĒ½ā±¾Ģā¹Ų¼ü£¬³£¼ūĪļÖŹ·ÖĄė·½·ØÓŠ£ŗ·ÖŅŗ”¢ÕōĮ󔢹żĀĖ”¢ÉųĪöµČ£¬»įøł¾ŻĪļÖŹµÄŠŌ֏єȔŗĻŹŹµÄ·ÖĄė·½·Ø£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| »Æѧ¼ü | ¼üÄÜ/£ØkJ•mol-1£© | »Æѧ¼ü | ¼üÄÜ/£ØkJ•mol-1£© |
| H-H | 436.0 | I-I | 153 |
| O=O | 497.0 | N=N | 946 |
| O-H | 463.0 | H-I | 297 |
| N-H | 391.0 |
| A£® | ĒāĘųµÄČ¼ÉÕČČĪŖ”÷H=-483kJ/mol | |
| B£® | H2£Øg£©+I2£Øg£©$\frac{200”ę}{\;}$2HI£Øg£©”÷H=-5kJ/mol | |
| C£® | N2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92kJ/mol | |
| D£® | ŌŚĻąĶ¬Ģõ¼žĻĀ£¬µČĮæµÄĒāĘųĶźČ«Č¼ÉÕŗĶÓėŃõĘų×é³ÉČ¼ÉÕµē³ŲŹ±£¬ģŹ±äĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”°ĄąīÕ”±¶ŌÓŚµÄĒāŃõ»ÆĪļ²»ČÜÓŚĖ® | B£® | ”°ĄąīÕ”±²»ÄÜŌŁæÕĘųÖŠĪČ¶Ø“ęŌŚ | ||
| C£® | ”°ĄąīÕ”±µ„ÖŹ²»ÓėĖ®·“Ó¦ | D£® | ”°ĄąīÕ”±µ„ÖŹÓŠ½ĻøßµÄČŪµć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪŖ±ćÓŚ¹Ū²ģĢśŌŚĀČĘųÖŠČ¼ÉÕµÄĻÖĻ󣬼ӓóĀČĘųµÄŹ¹ÓĆĮæ | |
| B£® | ÓĆŠ”ĶĮ£“śĢęæɵ÷½Śø߶ȵÄĶĖæ ½ųŠŠĶŗĶÅØĻõĖį·“Ó¦µÄŹµŃé | |
| C£® | ·ŁÉÕĖÜĮĻ”¢Ļš½ŗµČ·ĻĘśĪļŹĒ“¦Ąķ³ĒŹŠÉś²ś”¢Éś»īĄ¬»ųµÄÓŠŠ§·½·Ø | |
| D£® | ÓĆ¼ÓČČH2O2”¢Ļ”H2SO4ŗĶCu“śĢę¼ÓČČÅØH2SO4ŗĶCuÖĘČ”CuSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

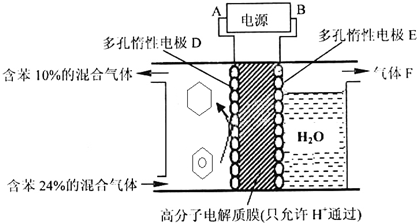
| A£® | Į÷³ĢÖŠµÄ·“Ӧȫ²æ¶¼ŹĒ·ĒŃõ»Æ»¹Ō·“Ó¦ | |
| B£® | MŹĒŃĪĖį | |
| C£® | µē½āČŪČŚMgO±Čµē½āČŪČŚMgCl2ÖĘ½šŹōĆ¾øü½ŚŌ¼ÄÜĮæ | |
| D£® | ²Ł×÷bÖ»ŹĒ¹żĀĖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 molĮņĖį¼ŲÖŠŅõĄė×ÓĖł“ųµēŗÉŹżĪŖNA | |
| B£® | ³£ĪĀĻĀ£¬2.7æĖĀĮÓė×ćĮæµÄĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬Ź§Č„µÄµē×ÓŹżĪŖ0.1NA | |
| C£® | ŌŚ³£ĪĀĻĀ£¬°Ń100 g CaCO3¼Óµ½1 LĖ®ÖŠ£¬ĖłµĆČÜŅŗÖŠµÄCa2+ŹżµČÓŚNA | |
| D£® | ŌŚ±ź×¼×“æöĻĀ£¬22.4 L CH4Óė18 g H2OĖłŗ¬ÓŠµÄ·Ö×ÓŹż¾łĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬ČŻĘ÷ÄŚÄ³Ņ»·“Ó¦ÖŠ£¬X”¢YµÄĪļÖŹŌŚĮæĖę·“Ó¦Ź±¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠ±ķŹöÖŠÕżČ·µÄŹĒ£Ø””””£©
ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬ČŻĘ÷ÄŚÄ³Ņ»·“Ó¦ÖŠ£¬X”¢YµÄĪļÖŹŌŚĮæĖę·“Ó¦Ź±¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠ±ķŹöÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2X?Y | B£® | t2Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬“ļµ½Ę½ŗā | ||
| C£® | t1Ź±£¬YµÄÅØ¶ČŹĒXµÄ2±¶ | D£® | t3Ź±£¬Õż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com