
【题目】W、X、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Z是非金属元素,W、X的最高价氧化物对应的水化物可以相互反应生成盐和水,向一定量的W的最高价氧化物对应的水化物溶液中逐滴加入XZ3溶液,生成的沉淀X(OH)3的质量随XZ3溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是()

A. d点对应的溶液中:K+、NH4+、CO32﹣、I﹣
B. c点对应的溶液中:Ag+、Ca2+、NO3﹣、Na+
C. b点对应的溶液中:Na+、S2﹣、SO42﹣、Cl﹣
D. a点对应的溶液中:Na+、K+、SO42﹣、HCO3﹣
【答案】C
【解析】试题分析:W、X、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Z是非金属元素,W、X的最高价氧化物对应的水化物可以相互反应生成盐和水,则W为Na元素,X为Al元素;X与Z形成XZ3溶液,则Z为Cl元素.向一定量的NaOH溶液中逐滴加入AlCl3溶液。由图可知,0~b,没有沉淀,故溶液中氢氧化钠有剩余,溶液中溶质为氢氧化钠、偏铝酸钠、氯化钠。b点时,氢氧化钠与氯化铝恰好完全反应,溶液中溶质为偏铝酸钠、氯化钠。b~c,沉淀增大,偏铝酸根与铝离子发生水解相互促进的反应,生成氢氧化铝沉淀,溶液中溶质为偏铝酸钠、氯化钠。c点时,沉淀达最大,偏铝酸根与铝离子恰好完全反应,溶液中溶质为氯化钠。c点以后,再加入氯化铝,沉淀不变,溶液中溶质为氯化铝、氯化钠。A、d点对应的溶液中含有Al3+,Al3+与C032-发生水解反应生成氢氧化铝沉淀、二氧化碳,不能大量共存,A错误;B、c点对应的溶液中含有Cl-,Cl-与Ag+反应生成氯化银沉淀,不能大量共存,B错误;C、b点对应的溶液中偏铝酸钠、氯化钠,离子之间不发生反应,可以大量共存,C正确;D、a点对应的溶液中含有氢氧化钠、偏铝酸钠、氯化钠,OH-与HCO3-发生反应生成碳酸根与水,不能大量共存,D错误,答案选C。


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
【题目】25℃时,向体积为 10 mL 的 0.1 mol/LNaOH溶液中逐滴加入0.1mol/LCH3COOH溶液,曲线如图所示。下列有关离子浓度关系的比较中,错误的是

A. a点处:c( Na+)>c(CH3COO-)>c(OH-)>c(H+)
B. b点处:c(CH3COOH)+c(H+ )=c(OH-)
C. c点处:c(CH3COOH)+c(CH3COO-)=2c(Na+)
D. NaOH溶液和CH3COOH溶液以任意比混合时:c( Na+)+c(H+)=c(OH-)+(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: X(g)+2Y(g) ![]() 3Z(g) ΔH=-a kJ·molˉ1(a>0)。下列说法正确的是
3Z(g) ΔH=-a kJ·molˉ1(a>0)。下列说法正确的是
A. 达到化学平衡状态时,Y 的正反应速率和 Z 的逆反应速率相等
B. 达到化学平衡状态时,X、Y、Z 的浓度之比为 1 : 2 : 3
C. 达到化学平衡状态时,反应放出的总热量一定小于 a kJ
D. 0.2 mol X 和 0.2 mol Y 充分反应生成 Z 的物质的量一定小于 0.3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发展洁净煤技术、利用CO2制备清洁能源等都是实现减碳排放的重要途径。
(1)将煤转化成水煤气的反应:C(s)+H2O(g)![]() CO(g)+H2(g)可有效提高能源利用率,若在上述反应体系中增大H2的浓度(其他条件保持不变),此反应的△H_____(填“增大”、“减小”或“不变”)。
CO(g)+H2(g)可有效提高能源利用率,若在上述反应体系中增大H2的浓度(其他条件保持不变),此反应的△H_____(填“增大”、“减小”或“不变”)。
(2)CO2制备甲醇:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H=-49.0 kJ·mol-1,在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。
CH3OH(g)+H2O(g)△H=-49.0 kJ·mol-1,在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。

①该反应化学平衡常数K的表达式是_________。
②0~9 min时间内,该反应的平均反应速率v(H2)=_________。
③在相同条件下,密闭容器的体积缩小至0.5 L时,此反应达平衡时放出的热量(Q)可能是_________(填字母序号)kJ。
a. 0<Q<29.5 b. 29.5<Q<36.75
c. 36.75<Q<49 d. 49<Q<98
④在一定条件下,体系中CO2的平衡转化率(![]() )与L和X的关系如图所示,L和X分别表示温度或压强。
)与L和X的关系如图所示,L和X分别表示温度或压强。

i. X表示的物理量是_________。
ii. 判断L1与L2的大小关系:L1________L2(填“<”,“=”或“>”),并简述理由:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由反应物 X 分别转化为 Y 和 Z 的能量变化如图所示。下列说法正确的是( )
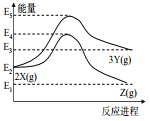
A.由 X→Z 反应的 ΔH<0 B.由 X→Y 反应的 ΔH=E5-E2
C.增大压强有利于提高 Y 的产率 D.升高温度有利于提高 Z 的产率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以浓缩海水为原料提取溴的部分流程如右图:下列说法正确的是

A. 海水需要浓缩,是因为海水中的Br2含量较低
B. 热空气的作用是将多余的Cl2吹出
C. 吸收塔中发生的反应是3Br2+3CO32-=5Br-+BrO3-+3CO2↑
D. 反应釜2中发生的反应是5Br-+BrO3-+3H2O=3Br2+6OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程.反应过程的示意图如下:
下列说法不正确的是

A. CO和O生成CO2是放热反应。
B. 在该过程中,CO分子中碳氧键没有断裂成C和O。
C. 在该过程中,O与CO中C结合形成共价键。
D. 状态Ⅰ→状态Ⅲ表示CO与O2反应的过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗铜中一般含有锌、铁、银、金等杂质.在如图3所示装置中,甲池的总反应方程式为:C2H5OH+3O2+4KOH=2K2CO3+5H2O 接通电路一段时间后,纯Cu电极质量增加了6.4 g。在此过程中,下列说法正确的是
A. 电子流向A→D→C→B
B. 乙池硫酸铜溶液的浓度不变
C. 甲池氧气消耗2.24 L
D. 甲池负极反应式为C2H5OH-12e﹣+16OH﹣=2CO32﹣+11H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解200mL KCl和CuSO4的混合溶液,经过一段时间后两极分别得到11.2L(标准状况下)气体。原混合溶液中KCl的物质的量浓度不可能为
A. 5mol/L B. 4mol/L C. 2.5mol/L D. 1mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com