


科目:高中化学 来源: 题型:
| A、c(H+)=1×10-3 mol?L-1 |
| B、c(OH-)=2×10-12 mol?L-1 |
| C、pH=2.3 |
| D、pH=3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Tl+最外层有3个电子 |
| B、铊位于第五周期ⅢA族 |
| C、Tl(OH)3与Al(OH)3相似,也是两性氢氧化物 |
| D、氧化性:Tl3+>Ag+>Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入碘水变蓝 |
| B、加入氯化铁溶液变蓝 |
| C、加入AgNO3溶液产生黄色沉淀 |
| D、加入氯水变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g?cm-3 | 溶解性 |
| A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水 |
| B | 17.9 | 290 | 1.26 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某温度时,在2L容器中X、Y、Z三种气体物质的量随时间的变化关系曲线如图所示.
某温度时,在2L容器中X、Y、Z三种气体物质的量随时间的变化关系曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
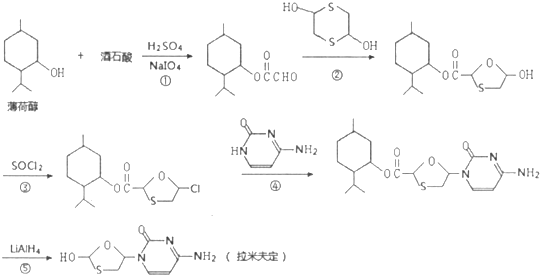
| HIO4 |
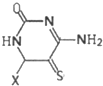 (其中X表示剩余的部分)
(其中X表示剩余的部分)查看答案和解析>>
科目:高中化学 来源: 题型:
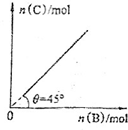 向盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)f4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的关系如图所示.下列说法正确的是( )
向盛有足量A的体积固定的密闭容器中加入B,发生反应:A(s)+2B(g)f4C(g)+D(g)△H<0.一定条件下达到平衡时,C的物质的量与加入的B的物质的量的关系如图所示.下列说法正确的是( )| A、升高温度,则图中θ>45° |
| B、平衡后再加入B,正反应速率增大,逆反应速率减小 |
| C、平衡时B的转化率为50% |
| D、平衡后再加入A,体系内气体密度增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com