
科目:高中化学 来源: 题型:选择题
| A. | 该反应中化合价变化的有N、C元素 | |
| B. | 当x=2时,每生成1 mol N2,转移电子数为4 mol | |
| C. | 等物质的量N2和CO2中,共价键的个数比为3:4 | |
| D. | 氧化剂与还原剂的物质的量之比为1:2时,NOx中氮元素的化合价为+4价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 食品化学家认为,当豆油被加热到油炸温度(180℃)时,会产生如图所示的高毒物质,许多疾病和这种有毒物质有关.下列关于这种有毒物质的判断错误的是( )
食品化学家认为,当豆油被加热到油炸温度(180℃)时,会产生如图所示的高毒物质,许多疾病和这种有毒物质有关.下列关于这种有毒物质的判断错误的是( )| A. | 该物质的分子式为C9H16O2 | |
| B. | 该物质能发生银镜反应 | |
| C. | 该物质能发生水解反应 | |
| D. | 该物质1mol最多可以和2mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
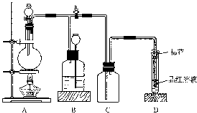 如图所示装置为铜跟浓硫酸反应制取二氧化硫的实验装置:
如图所示装置为铜跟浓硫酸反应制取二氧化硫的实验装置:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9.2 g | B. | 10.6 g | C. | 6.2 g | D. | 4.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 64 g SO2含有氧原子数为NA | |
| B. | 物质的量浓度为0.5mol/LAl2(SO4)3溶液,含有SO42-离子数为1.5NA | |
| C. | 标准状况下,22.4 LSO3的分子数为NA | |
| D. | 常温常压下,14 g N2含有分子数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com