
【题目】0.5molCO2中含有_______个CO2分子,_______mol氧原子, ______个碳原子,CO2的质量为__________ g,标况下体积为_________ L。![]() 11.1g的ACl2中含有0.2molCl-,ACl2的物质的量是__________,ACl2的摩尔质量是__________,A的相对原子质量是________。
11.1g的ACl2中含有0.2molCl-,ACl2的物质的量是__________,ACl2的摩尔质量是__________,A的相对原子质量是________。
科目:高中化学 来源: 题型:
【题目】PbCl2是一种重要的化工材料,常用作助溶剂、制备铅黄等染料。工业生产中利用方铅矿精矿(主要成分为PbS,含有FeS2等杂质)和软锰矿(主要成分为MnO2)制备PbCl2的工艺流程如下图所示。

已知:i.PbCl2微溶于水
ii.PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq)△H>0
PbCl42-(aq)△H>0
(1)浸取过程中MnO2与PbS发生如下反应,请将离子反应补充完整并配平:_____
______+___Cl-+___PbS+___MnO2=___PbCl2+__SO42-+_____ +_____
(2)由于PbCl2微溶于水,容易附着在方铅矿表面形成“钝化层”使反应速率大大降低,浸取剂中加入饱和NaCl溶液可有效避免这一现象,原因是__________。
(3)调pH的目的是____________。
(4)沉降池中获得PbCl2采取的措施有_________。
(5)通过电解酸性废液可重新获得MnO2,装置示意图如下:

①在_____极(填“a”或“b”)获得MnO2,电极反应为_______________。
②电解过程中发现有Cl2产生,原因可能是_____________(用化学用语表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将8.4g Fe投入浓硝酸中,产生红棕色气体A,把所得溶液减压蒸干,得到30g Fe(NO3)2和Fe(NO3)3的混合物,将该固体隔绝空气在高温下加热,得到红棕色的Fe2O3和气体B,A、B气体混合通入足量水中得到硝酸和NO,在标准状况生成NO气体的体积为
A. 1120mL B. 2240mL C. 3360mL D. 4480mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:_____、____。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。
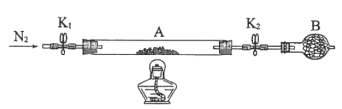
①仪器B的名称是____________________。
②将下列实验操作步骤正确排序___________________(填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③根据实验记录,计算绿矾化学式中结晶水数目x=________________(列式表示)。若实验时按a、d次序操作,则使x__________(填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
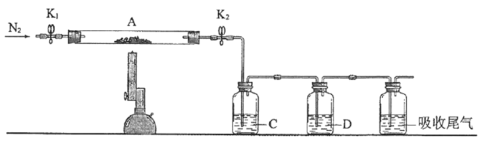
①C、D中的溶液依次为______(填标号)。C、D中有气泡冒出,并可观察到的现象分别为______。
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②检验残留固体是否还存在硫酸亚铁的方法为_____,并写出对应离子方程式____
③写出硫酸亚铁高温分解反应的化学方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,在两个容积相同的容器中,一个盛有CO2气体,另一个盛有O2和N2的混和气体,则两容器内的气体一定具有相同的( )
A.密度B.原子数C.质量D.分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制备氯气并验证氯气性质的装置(其中夹持装置已省略)。

已知:装置A是氯气的发生装置,反应的化学方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O。据此回答下列问题:
(1)装置B中饱和食盐水的作用是________;长颈漏斗的作用是__________。
(2)装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是: 湿润的有色布条、 无水氯化钙、干燥的有色布条,请你推测Ⅰ、Ⅲ处的现象依次为:______,_____。
(3)装置D的作用是___________,则烧杯中的溶液是______,写出所发生反应的化学方程式: ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到目的的是( )

A. 装置①依据两容器内气体颜色变化,不能判断反应2NO2(g)![]() N2O4(g)平衡移动的方向
N2O4(g)平衡移动的方向
B. 装置②依据U管两边液面的高低判断Na和水反应的热效应
C. 装置③测定中和热
D. 装置④依据褪色快慢比较浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物J是一种防止血管中血栓形成与发展的药物,其合成路线如图所示(部分反应条件略去)。
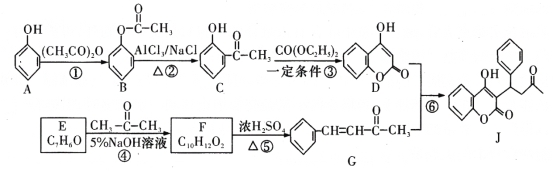
请回答下列问题:
(1)B的名称为______________,反应⑥的反应类型是__________。
(2)J含有_______种官能团。F的结构简式是_____________。
(3)反应③的化学方程式为____________________________________________-。
(4)写出同时满足下列条件的F的同分异构体的结构简式:______________(至少写两种)。
①苯环上只有两个处于对位的取代基;
②1 mol该有机物能与含2 mol NaOH的溶液恰好完全反应。
(5)参照D的合成路线,设计一种以![]() 为原料制备
为原料制备 的合成路线__________。
的合成路线__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池(MFC)是一种现代化氨氮去除技术。下图为MFC碳氮联合同时去除的转化系统原理示意图。下列说法正确的是
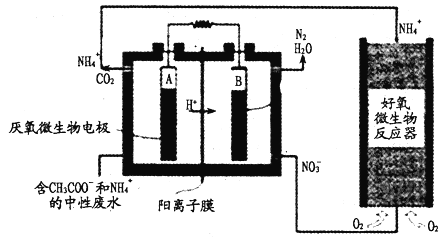
A. 好氧微生物反应器中反应为:NH4++2O2==NO3-+2H++H2O
B. B极电势比A极电势低
C. A极的电极反应式CH3COO-+8e-+2H2O==2CO2+7H+
D. 当电路中通过1mol电子时,理论上总共生成2.24LN2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com