
下列有关胶体的说法错误的是:
A.胶粒可以透过滤纸,不能透过半透膜
B.采用喷雾型药剂形成一定大小的液珠,可有效提高药物疗效
C.冶金工业的矿粒除尘利用了丁达尔效应
D.空气中的雾霾现象体现了胶体的存在
科目:高中化学 来源:2016届宁夏石嘴山三中高三下四模理综化学试卷(解析版) 题型:填空题
二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,被称为“第4代消毒剂”。工业上可采用氯酸钠(NaClO3)或亚氯酸钠(NaClO2)为原料制备ClO2。
(1)亚氯酸钠也是一种性能优良的漂白剂,但在强酸性溶液中会发生歧化反应,产生ClO2气体,离子方程式为___________________________;向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为相同pH的硫酸,开始时反应缓慢,稍后一段时间产生气体速率迅速加快。产生气体速率迅速加快的原因是 。
(2)化学法可采用盐酸或双氧水还原氯酸钠制备ClO2。用H2O2作还原剂制备的ClO2更适合用于饮用水的消毒,其主要原因是 。
(3)电解法是目前研究最为热门的生产ClO2的方法之一。如图所示为直接电解氯酸钠、自动催化循环制备高纯ClO2的实验。
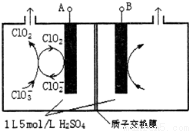
①电源负极为___________________极(填A或B)
②写出阴极室发生反应的电极反应式和离子方程式
_______________________ ___ ; 。
③控制电解液H+不低于5mol/L,可有效防止因H+浓度降低而导致的ClO2—歧化反应。若两极共收集到气体22.4L(体积已折算为标准状况,忽略电解液体积的变化和ClO2气体溶解的部分),此时阳极室与阴极室c(H+)之差为_________________。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三下学期冲刺模拟理综化学A卷(解析版) 题型:实验题
亚氯酸钠(NaClO2)是重要漂白剂。某化学兴趣小组同学展开对亚氯酸钠(NaClO2)的研究。
实验Ⅰ:制取NaClO2晶体
已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2•3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。Ba(ClO2)2可溶于水。
利用下图所示装置进行实验。

(1)装置②中产生ClO2气体的化学方程式为 。
(2)从装置④反应后的溶液获得晶体NaClO2的操作步骤为:
①减压,55℃蒸发结晶;②趁热过滤;③ ;④低于60℃干燥,得到成品。过滤用到的玻璃仪器有 。
(3)设计实验检验所得NaClO2晶体是否含有杂质Na2SO4,操作是: 。
(4)反应结束后,关闭K2、打开K1,装置①的作用是 ;如果撤去D中的冷水浴,可能导致产品中混有的杂质是 。
实验Ⅱ:测定某亚氯酸钠样品的纯度。
设计如下实验方案,并进行实验:
①准确称取所得亚氯酸钠样品m g于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO2-+ 4I-+4H+ =2H2O+2I2+Cl-)。将所得混合液配成100mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,用c mol•L-1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为V mL(已知:I2 +2S2O32-=2I-+S4O62-)。
(5)滴定中使用的指示剂是 ,达到滴定终点时的现象为 。
(6)样品中NaClO2的质量分数为 (用含m、c、V的代数式表示,式量:NaClO2 90.5)。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三第九次月考化学试卷(解析版) 题型:填空题
(1)在298K,100kPa时.CH4的燃烧热是890.0kJ/mol,写出该反应的热化学方程式__________。现有CH4和CO的混合气体0.75mol,完全燃烧后,生成CO2气体和18g液态水,共放出QkJ热量(假定热量未损失),则CH4和CO的物质的量的比为__________。
(2)利用甲烷的燃烧反应设计一个燃料电池,用氢氧化钾溶液作电解质溶液.多孔石墨作电极,在电极上分别通入甲烷和氧气,通入甲烷气体的电极上发生的电极反应是___________,当电路中转移12mol电子时,实际提供的电能是890.0kJ,则该电池的能量转化效率是__________。
(3)将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中形成如图装置:

①当开关K1闭合,则铁发生电化学腐蚀中的__________腐蚀。
②当开关K2闭合,则总反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三第九次月考化学试卷(解析版) 题型:选择题
设NA为阿佛加德罗常数.下列说法正确的是
A.lmol羟基和lmol氢氧根离子所含的电子数均为10NA
B.0.lmol/L乙酸溶液中所含醋酸根离子的数目小于0.1NA
C.当合成氨反应达到平衡时,表明每生成6NA个N-H键的同时必生成3NA个H-H键
D.46g由NO2和N2O4组成的混合气体中所含的原子数为3NA
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三5月高考模拟理综化学试卷(解析版) 题型:填空题
由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。化合物有E最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯.玉米淀粉等发酵制得,E的钙盐是人们喜爱的补钙剂之一。

已知: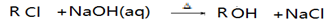
(1)D中所含官能团名称。E→G的反应类型为_________。
(2)聚合物F的结构简式。聚合物G的结构简式_________
(3)在一定条件下,两分子E在浓硫酸作用下形成一种六元环状化合物,该化合物的结构简式是_________。
(4)B转化为C的化学反应方程式是_________。
(5)下列四种化合物与E互为同分异构体的是_________。
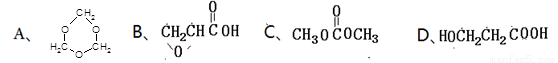
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.氢能将是二十一世纪的重要能源,推广应用氢能最关键技术是高容量储氢材料的研制
B.纳米TiO2光触媒技术制成的“木地板精油”能将水气转化为活性氧,由此可推测TiO2光触媒技术制成的“木地板精油可以有效降解甲醛、苯、氨等居室污染物
C.高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强酸、强碱都会“断路”
D.门捷列夫提出的元素周期律为发现新元素、合成新材料提供了新思路
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中文科化学试卷(解析版) 题型:选择题
下列物质的溶液不能与Al(OH)3反应的是
A.NH3·H2O B.NaOH C.HCl D.H2SO4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一下期中化学试卷(解析版) 题型:填空题
最新报道,我国科学家通过与多个国家进行科技合作,成功研发出铯(Cs)原子喷泉钟,使我国时间频率基准的精度从30万年不差1秒提高到600万年不差1秒,标志着我国时间频率基准研究进入世界先进行列。已知铯位于元素周期表中第六周期第ⅠA族,根据铯在元素周期表中的位置,推断下列内容:
(1)铯的原子核外共有_____个电子层,最外层电子数为______,铯的原子序数为______。
(2)铯单质与水剧烈反应,放出____色气体,请写出反应的化学方程式:_________________。
(3)预测铯单质的还原性比钠单质的还原性________(填“弱”或“强”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com