
下列叙述中,可以说明金属甲比乙活泼性强的是()
A. 将甲乙作电极组成原电池时甲是负极
B. 甲和乙用导线连接插入稀盐酸溶液中,乙溶解,甲上有H2气放出
C. 在氧化还原反应中,甲比乙失去的电子多
D. 同价态的阳离子,甲比乙的氧化性强
考点: 原电池和电解池的工作原理;常见金属的活动性顺序及其应用.
专题: 电化学专题.
分析: A、在原电池中,负极金属的活泼性比正极上的活泼;
B、在原电池中,负极金属溶解,正极上会产生气泡或是生成金属单质;
C、金属失电子的多少不能说明金属的活泼性;
D、金属阳离子的氧化性越强,单质的还原性越弱.
解答: 解:A、将甲乙作电极组成原电池时甲是负极,可以说明金属甲比乙活泼性强,故A正确;
B、甲和乙用导线连接插入稀盐酸溶液中,乙溶解,甲上有H2气放出,说明金属甲比乙活泼性弱,故B错误;
C、在氧化还原反应中,甲比乙失去电子的能力强可以说明金属甲比乙活泼性强,金属失电子的多少不能说明金属的活泼性,故C错误;
D、同价态的阳离子,甲比乙的氧化性强,说明金属甲比乙活泼性弱,故D错误.
故选A.
点评: 本题考查学生金属的活泼性强弱的判断方法,注意原电池原理的应用是关键,难度不大.


科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的数值,下列说法正确的是()
A. 标准状况下,22.4LCCl4含有NA个分子
标准状况下,22.4LCCl4含有NA个分子
B. 0.1molAlCl3完全转化为胶体,生成胶体粒子的数目为0.l NA个
C. 常温常压下46gNO2和N2O4的混合气体含有3NA个原子
D. 0.1molCl2与足量冷的NaOH溶液反应,转移电子数为0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生将一小块钠投入滴有酚酞的水中,此实验能证明钠下面4点性质中的()
①钠比水轻
②钠的熔点较低
③钠与水反应在时要放出热量
④钠与水反应后溶液呈碱性.
A. ①④ B. ①②④ C. ①③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
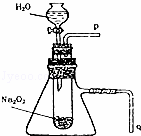
用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.
(1)由实验现象所得出的有关Na2O2和H2O反应的结论是 (填序号)
a.反应放热 b.棉花在空气中可以自燃
c.有O2生成 d.Na2O2在空气中可以自燃
(2)写出Na2O2和H2O反应的化学方程式 .
(3)某校研究性学习小组拟用如图装置进行实验,以证明上述结论.为验证得到的气体产物所进行实验操作方法及现象是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
将Mg条、Al条平行插入一定浓度的NaOH溶液中,用导线、电流计连接成原电池,此电池工作时,下列叙述中正确的是()
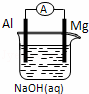
A. Mg比Al活泼,Mg 失去电子被氧化成Mg2+
B. 负极反应式为:Al+4OH﹣﹣3e﹣=AlO2﹣+2H2O
C. 该电池的内外电路中,电流均是由电子定向移动形成的
D. Al是电池阴极,开始工作时溶液中会立即有白色沉淀析出
查看答案和解析>>
科目:高中化学 来源: 题型:
将Fe片和Al片放在盛有NaCl溶液(其中滴入酚酞)的表面皿中,如图表示,最先观察到变红色的区域为()
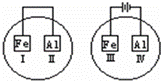
A. II和Ⅳ B. Ⅱ和Ⅲ C. Ⅰ和Ⅲ D. Ⅰ和Ⅳ
查看答案和解析>>
科目:高中化学 来源: 题型:
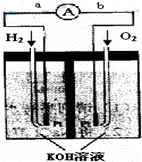
氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b 表示).
(2)负极反应式为 .
(3)电极表面镀铂粉的原因为增
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能.因此,大量安全储氢是关键技术之一.金属锂是一种重要的储氢材料,吸氢和放氢原理如下:Ⅰ.2Li+H2 2LiHⅡ.LiH+H2O═LiOH+H2↑
2LiHⅡ.LiH+H2O═LiOH+H2↑
①反应Ⅰ中的还原剂是Li,反应Ⅱ中的氧化剂是H2O.
②用锂吸收224L(标准状况)H2,再由生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 .
③若改用熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极.已知负极的电极反应是CH4+4CO32﹣﹣8e﹣=5CO2+2H2O.则正极的电极反应是 .为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,此电池工作时必须有部分A物质参加循环,则A物质的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应N2+3H2⇌2NH3的正、逆反应速率可用各反应物和生成物浓度的变化来表示.下列各关系中能说明反应已达到平衡状态的是()
A. 3v正(N2 )=v正(H2 ) B. v正(N2 )=v逆(NH3)
C. 2v正(H2 )=3v逆(NH3) D. v正(N2 )=3v逆(H2 )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com