
【题目】自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。

I.请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)碳酸钙悬浊液中分离出碳酸钙___;
(2)氯化钠溶液中分离出氯化钠___;
(3)分离植物油和水___;
(4)海水淡化___;
(5)从碘水中分离出I2___。
II.碘水中提取碘单质的方法如下:
(1)萃取分液
①下列可作为碘水中提取碘单质萃取剂的是___;
A.酒精 B.苯
②分液漏斗在使用前必须先___;
③查资料得知:ρ(H2O)>ρ(苯)>ρ(酒精),若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应由分液漏斗的___端口放出,有机层应由分液漏斗的___端口放出(此问填“上”或者“下”)。
(2)蒸馏
①装置A中a的名称是___,冷凝装置中冷凝水应该___口进(填“上”或“下”),这样做的目的是___。
②已知碘和四氯化碳的熔沸点数据如下表
熔点 | 沸点 | |
碘 | 113.7℃ | 184.3℃ |
四氯化碳 | -22.6℃ | 76.8℃ |
若用蒸馏法分离碘和四氯化碳的混合物,锥形瓶中先收集到的物质的名称是___。
【答案】B D C A C B 检查是否漏液 下 上 蒸馏烧瓶 下 使水充满冷凝管,水流方向与蒸汽方向相反,冷凝效果更好 四氯化碳
【解析】
I. 由装置图可知A为蒸馏,常用于分离沸点不同的液体混合物;B为过滤,常用于分离固液混合物;C为萃取分液;D为蒸发,结合混合物的性质的异同选择分离方法
II.(1)①碘水中提取碘单质,选取的萃取剂不能与溶剂水相溶;
②分液漏斗有旋塞,使用分液漏斗前必须检查其是否漏水;
③苯为有机溶剂,则有机层的密度小于水溶液,分层后碘的苯溶液在上层、水溶液在下层,上层液体从分液漏斗口放出,下层液体从下口放出;
(2)①蒸馏装置中,冷凝管的通水方向采用逆向通水法,确保冷凝效果较好;
②蒸馏过程中,沸点越低,则优先在锥形瓶中收集到,据此判断锥形瓶中先收集到的物质的名称。
I. (1)碳酸钙悬浊液中分离出碳酸钙,碳酸钙不溶于水,可以通过过滤操作分离,则应该选用装置B;
(2)氯化钠溶液中分离出氯化钠,需要通过蒸发操作完成,应该选用装置D;
(3)分离植物油和水,二者互不相溶,可以通过分液操作完成,应该选用装置C;
(4)海水淡化,可以通过蒸馏操作完成,所以应该选用装置A;
(5)从碘水中分离出I2,可以通过萃取分液操作完成,所以应该选用装置C;
II. (1)①碘水中提取碘单质,需要通过萃取方法,选取的萃取剂不能与水相溶,所以不能选用A酒精,可以选用苯,故答案为:B;
②分液漏斗有瓶塞和旋塞,检查分液漏斗前必须检查分液漏斗是否漏液;
③由于ρ(H2O)>ρ(苯),若用苯为萃取剂萃取碘水中的碘单质,有机层在上方、水层在下层,则分液时,水层应由分液漏斗的下端口放出,有机层应由分液漏斗的上端口放出;
(2)①如图,A上午名称为蒸馏烧瓶,给冷凝管通水时,通常采用逆向通水,即:从冷凝管的下口进水,冷凝效果会更好;
②根据表中碘单质和四氯化碳的沸点可知,四氯化碳的沸点较低,则四氯化碳优先被蒸出,锥形瓶中先收集到的物质为四氯化碳。


科目:高中化学 来源: 题型:
【题目】(1)实验室用金属铜和稀硝酸制取NO的离子方程式为______________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。

①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填序号)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是__________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是______________________________________________________。
②让反应停止的操作方法及原因是__________________________________________。
(4)以下收集NO气体的装置,合理的是________(填序号)。
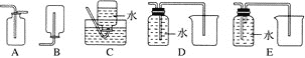
(5)将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
①NO的体积为________ L,NO2的体积为________ L。
②待产生的气体全部释放后,向溶液中加入VmLamol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种短周期元素的位置如图所示(其中乙、丙、丁的位置未标出)。
![]()
已知四种元素的原子序数之和为36,乙的原子序数与甲、丁原子序数之和相等。
(1)甲元素在周期表中的位置为______________。
(2)丙、丁可形成AB2型化合物,其化学式为________。
(3)丙是自然界中形成化合物种类最多的元素,则丙是________(填名称),其单质与甲元素的最高价氧化物对应水化物的浓溶液共热时反应的化学方程式是______________________。
(4)若甲、乙、丙、丁四种元素两两化合时,丁与其他三种元素得到的化合物种类最多,则丁是________(填元素符号),写出这些化合物中任意两种符合以下条件的化学式______________________
(①原子个数比为1∶2;②分子中价电子总数为偶数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是( )
A. SO3+ H2O= H2SO4 B. NH4Cl ![]() NH3
NH3![]() +HCl
+HCl![]()
C. Fe+CuSO4= FeSO4+Cu D. NaOH+HNO3=NaNO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是
A. CaCO3+2HCl=CaCl2+CO2↑+ H2O
B. CaO+H2O=Ca(OH)2
C. 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
D. CaCO3![]() CaO+CO2↑
CaO+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.3mol/LNaOH溶液480mL。根据溶液的配制情况回答下列问题。
(1)如图所示,配制上述溶液还需用到的玻璃仪器是__(填仪器名称)。
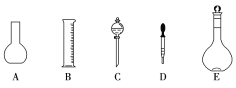
(2)下列操作中,容量瓶所不具备的功能有___(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
(3)根据计算,用托盘天平称取NaOH的质量为___g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度___(填“偏大”“不变”或“偏小,下同)。若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种药物中间体,合成 G的部分流程如下:

请回答下列问题:
(1)G物质中的含氧官能团的名称是___________、____________。
(2)上述⑤变化过程的反应类型是_____________。
(3)反应A→B的化学方程式为________________________________________。
(4)写出满足下列条件的C的同分异构体的结构简式:_______________________。
Ⅰ. 苯环上只有两种取代基。
Ⅱ. 分子中只有4种不同化学环境的氢。
Ⅲ. 能与NaHCO3反应生成CO2。
(5)根据已有知识并结合相关信息,写出以![]() 和乙酸酐为原料制备
和乙酸酐为原料制备![]() 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:H2C=CH2
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH__________
CH3CH2OH__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被称之为“软电池”的纸质电池,其电池总反应为Zn+2MnO2+H2O![]() ZnO+2MnO(OH)。下列说法正确的是( )
ZnO+2MnO(OH)。下列说法正确的是( )
A.该电池的正极为锌
B.该电池反应中二氧化锰起催化剂作用
C.当65 g Zn完全溶解时,流经电极的电子为1mol
D.电池正极反应式为2MnO2+2e-+2H2O![]() 2MnO(OH)+2OH-
2MnO(OH)+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各图的叙述不正确的是( )
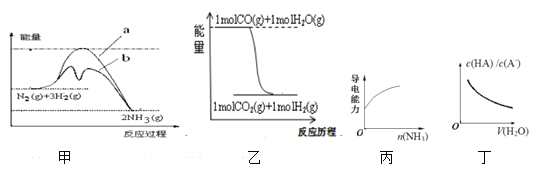
A.图甲中曲线b表示工业合成氨中加入铁触媒(催化剂)的能量变化曲线
B.根据图乙可知在该条件下:CO2(g)+H2 (g)=CO(g)+H2O(g) △H<0
C.图丙中曲线表示向1.0mol·L-1的醋酸溶液中通入氨气,溶液导电能力的变化情况
D.图丁中曲线表示常温下向弱酸HA的稀溶液中加水稀释时,c(HA)/c(A-)的变化情况
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com