
【题目】(题文)无水AlCl3可用作有机合成的催化剂、食品膨松剂等。
已知:①AlCl3、FeCl3分别在183 ℃、315 ℃时升华;②无水AlCl3遇潮湿空气变质。
Ⅰ. 实验室可用下列装置制备无水AlCl3。
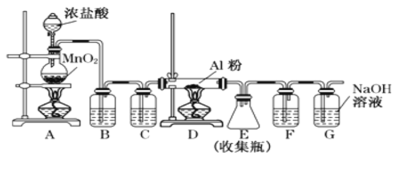
(1)组装好仪器后,首先应_____________,具体操作为_____________________
(2)装置 B中盛放饱和NaCl溶液,该装置的主要作用是__________________。装置C中盛放的试剂是________________。装置F中试剂的作用是__________。若用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为_______
(3)将所制得的无水AlCl3配制溶液时需加入盐酸的目的是_________
Ⅱ. 工业上可由铝土矿(主要成分是Al2O3和Fe2O3)和焦炭制备,流程如下:
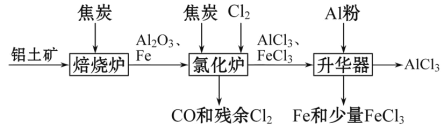
(1)氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式为___________________
(2)700 ℃时,升华器中物质充分反应后降温实现FeCl3和AlCl3的分离。温度范围应为_______
a.低于183 ℃ b.介于183 ℃和315 ℃之间 c.高于315 ℃
(3)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。
![]()
计算该样品中AlCl3的质量分数________(结果用m、n表示,不必化简)。
【答案】检查装置气密性关闭装置A中分液漏斗的活塞,向G中加入蒸馏水没过导管,微热A,一段时间后若G中有气泡冒出,停止加热后导管内有水柱,则气密性良好;除HCl浓硫酸吸收水,防止无水AlCl3遇潮湿空气变质碱石灰抑制铝离子水解Al2O3+3Cl2+3C![]() 2AlCl3+3COb
2AlCl3+3COb![]() ×100%或
×100%或![]() ×100%
×100%
【解析】
I.(1)此实验中有气体的参与,因此实验之前首先检验装置的气密性;检验气密性的方法,一般采用加热法和液差法两种;(2)利用题中信息,可以完成;(3)从水解的应用角度进行分析;II.(1)根据流程的目的,焦炭在高温下转化成CO,然后根据化合价升降法进行配平;(2)利用AlCl3和FeCl3升华的温度,进行分析;(3)根据元素守恒进行计算。
I.(1)装置A制备氯气,因此需要检验装置的气密性,本实验的气密性的检验方法是:关闭装置A中分液漏斗的活塞,向G中加入蒸馏水没过导管,微热A,一段时间后若G中有气泡冒出,停止加热后导管内有水柱,则气密性良好;(2)A中制备的氯气中混有HCl和H2O,HCl能与Al发生反应,AlCl3遇水易变质,因此必须除去HCl和H2O,装置B的作用是除去氯气中的HCl,装置C的作用是除去水蒸气,即盛放的是浓硫酸。因为AlCl3遇水易变质,因此装置F的作用是防止G中水蒸气进去E装置,使AlCl3变质;氯气有毒,需要吸收尾气,因此装置G的作用是吸收多余的氯气,防止污染空气,如果G和F改为一个装置,应用干燥管,盛放试剂为碱石灰;(3)AlCl3属于强酸弱碱盐,Al3+发生水解:Al3++3H2O![]() Al(OH)3+3H+,加入盐酸的目的是抑制Al3+的水解;II.(1)流程的目的是制备AlCl3,因此氯化炉中得到产物是AlCl3,焦炭在高温下,生成CO,因此反应方程式为Al2O3+3Cl2+3C
Al(OH)3+3H+,加入盐酸的目的是抑制Al3+的水解;II.(1)流程的目的是制备AlCl3,因此氯化炉中得到产物是AlCl3,焦炭在高温下,生成CO,因此反应方程式为Al2O3+3Cl2+3C![]() 2AlCl3+3CO;(2)AlCl3、FeCl3分别在183 ℃、315 ℃时升华,因此进行分离,需要控制温度在183℃到315℃之间,故选项b正确;(3)根据铝元素守恒,AlCl3的物质的量为n×2/102mol,则AlCl3的质量为133.5×2×n/102g,即AlCl3的质量分数为
2AlCl3+3CO;(2)AlCl3、FeCl3分别在183 ℃、315 ℃时升华,因此进行分离,需要控制温度在183℃到315℃之间,故选项b正确;(3)根据铝元素守恒,AlCl3的物质的量为n×2/102mol,则AlCl3的质量为133.5×2×n/102g,即AlCl3的质量分数为![]() ×100%或
×100%或![]() ×100%。
×100%。


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,其中NH3被氧化为常见的无毒物质。下列说法错误的是( )

A. 溶液中OH-向电极a移动
B. 电极b上发生还原反应
C. 负极的电极反应为2NH3-6e-+6OH-![]() N2+6H2O
N2+6H2O
D. 理论反应消耗的NH3与O2的物质的量之比为3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤和汽车尾气是造成空气污染的原因之一,雾疆天气肆虐给人类健康带来了严重影响,化学在解决雾霾污染中发挥了重要作用。
(1)煤燃烧产生的烟气中含有氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
己知:
CH4(g)+2NO2(g) ![]() N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1
N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1
2NO2(g) ![]() N2O4(g) △H=-56.9kJ·mol-1
N2O4(g) △H=-56.9kJ·mol-1
H2O(g)=H2O(l) △H=-44.0kJ·mol-1
①写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式________________。
②反应CH4(g)+2NO2(g) ![]() N2(g)+CO2(g)+2H2O(l)在恒温恒容容器中达到平衡,下列叙述不能作为判断该反应达到平衡状态标志的是___________。
N2(g)+CO2(g)+2H2O(l)在恒温恒容容器中达到平衡,下列叙述不能作为判断该反应达到平衡状态标志的是___________。
A.容器中的压强不变 B.混合气体的密度不变
C.2v正(NO2)= v 逆(N2) D.c(CH4)= c(N2)
(2)CO、CO2 是火力发电厂及汽车尾气的主要成分,为减少对环境造成的影响,采用以下方法将其资源化利用。
①以CO 为电极燃料,以熔融K2CO3为电解质,和O2组成燃料电池。请写出该电池的负极电极反应式_____________________。
②在铝矾土作催化剂、773K条件下,3molCO与1.5molSO2反应生成3molCO2和0.75mol硫蒸气,该反应可用于从烟道气中回收硫,写出该反应的化学方程式_______________。
③在汽车的排气管上增加一个补燃器,并不断补充O2使其浓度保持为4.0×10-4mol·L-1,发生反应2CO(g)+O2(g) ![]() 2CO2(g)。某温度下测得汽车尾气中CO、CO2 气体的浓度分别为2.0×10-6 mol·L-1、4.0×10-4 mol·L-1,则该条件下反应的平衡常数K=___________。
2CO2(g)。某温度下测得汽车尾气中CO、CO2 气体的浓度分别为2.0×10-6 mol·L-1、4.0×10-4 mol·L-1,则该条件下反应的平衡常数K=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着现代工业的发展,能源问题已经越来越引起人们的重视。科学家预言,未来最理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)用适当的催化剂水解成葡萄糖,再将葡萄糖转化为乙醇,用作燃料。
(1)写出绿色植物的秸秆转化为乙醇的化学方程式:
①____________________________________________;
②____________________________________________。
(2)乙醇除用作燃料外,还可以用它合成其他有机物。如图主要是以乙醇为起始原料的转化关系图,请在图中填上相应物质的结构简式___________________________。
![]()

(3)写出上面转化关系图中由CH2OHCH2OH![]() C4H4O4的化学方程式 (有机物用结构简式表示)________________________________________________________________。
C4H4O4的化学方程式 (有机物用结构简式表示)________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】南昌西汉海昏侯墓考古发现震惊全国,在打开内棺时,为了防止丝织品被氧化,需要充入一定的保护气体,这种气体是( )
A. H2 B. CO C. SO2 D. N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“摇摇冰”是一种即用即冷的饮料。吸食时将饮料罐隔离层中的化学物质和水混合后摇动即会制冷。该化学物质是
A.氯化钠B.固体硝酸钾C.生石灰D.固体氢氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氨及铵盐的性质叙述中,正确的是
A. 氨气可用排水法收集
B. 氯化铵固体加热容易分解
C. 氨气和酸相遇都能产生白烟
D. 实验室用氢氧化钠溶液和氯化铵溶液加热制NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯佐卡因是局部麻醉药,常用于手术后创伤止痛、溃疡痛等,其结构简式为 。下列关于苯佐卡因的叙述正确的是
。下列关于苯佐卡因的叙述正确的是
A. 分子式为C9H14NO2
B. 苯环上有2个取代基,且含有硝基的苯佐卡因的同分异构体有9种
C. 1mol该化合物最多与4mol氢气发生加成反应
D. 分子中将氨基转化成硝基的反应为氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com