
| A. | 2H2O2═2H2O+O2↑ | B. | 2FeCl2+Cl2═2FeCl3 | ||
| C. | Pb2++2Cl-═PbCl2↓ | D. | Sn2++2Fe3+═Sn4++2Fe2+ |
分析 氧化还原反应的实质为电子的转移,特征为化合价升降,则反应中存在化合价变化的反应为氧化还原反应,没有化合价变化的反应为非氧化还原反应,据此进行解答.
解答 解:A.2H2O2═2H2O+O2↑为分解反应,反应中氧元素化合价变化,属于氧化还原反应,故A不选;
B.反应2FeCl2+Cl2═2FeCl3中铁元素合价变化,属于氧化还原反应,故B不选;
C.Pb2++2Cl-═PbCl2↓中不存在化合价变化,不属于氧化还原反应,故C选;
D.Sn2++2Fe3+═Sn4++2Fe2+中存在Sn、Fe元素的化合价变化,属于氧化还原反应,故D不选;
故选C.
点评 本题考查了氧化还原反应的判断,题目难度不大,明确氧化还原反应的实质、特征为解答关键,注意掌握常见反应类型与氧化还原反应的关系,试题有利于提高学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 含NaOH 0.1mol | B. | 浓度为 1mol/L | C. | 含NaOH 4g | D. | 浓度为 0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸---蒸馏 | B. | 饱和食盐水---蒸馏 | ||
| C. | 饱和碳酸氢钠溶液---分液 | D. | 饱和碳酸钠溶液---分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
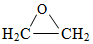 +CaCl2+2H2O
+CaCl2+2H2O +CaCl2+H2O
+CaCl2+H2O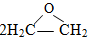
| A. | 12.7% | B. | 25.4% | C. | 50.8% | D. | 76.2% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同质量的铝,分别与足量的盐酸和氢氧化钠溶液反应放出的氢气体积一定不相同 | |
| B. | 56gFe与足量盐酸反应转移电子数为3NA | |
| C. | 任何条件下,22.4LNH3与18gH2O所含电子数均为10NA | |
| D. | 46gNO2和N2O4的混合物含有的原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
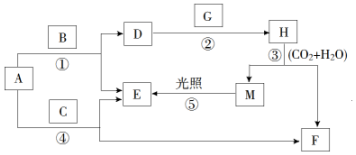
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在NaHS溶液中滴人少量CuCl2溶液,产生黑色沉淀,HS-水解程度增大,pH增大 | |
| B. | 常温下,由于HCO3-水解显碱性,所以饱和NaHCO3溶液显碱性 | |
| C. | 泡沫灭火器是利用Al2(SO4)3溶液与饱和NaHCO3溶液混合产生气体 | |
| D. | 配制氯化铝溶液时,先将氯化铝溶于浓硫酸,再加水稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
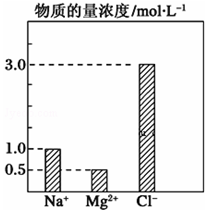 在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com