
| A.气体A为二氧化硫和氢气的混合物 |
| B.气体A中二氧化硫和氢气的体积比为4:1 |
| C.反应中共消耗锌97.5g |
| D.反应中共转移电子1.5mol |


科目:高中化学 来源:不详 题型:单选题
| A.容量瓶中原有少量蒸馏水 |
| B.溶液从烧杯转移到容量瓶中后没有洗涤烧杯 |
| C.滴管加水时,有少量水滴到容量瓶外 |
| D.加水未达到刻度线 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
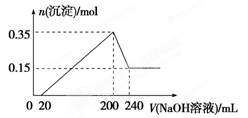
| A.镁和铝的总质量为9 g |
| B.最初20 mL NaOH溶液用于中和过量的稀硫酸 |
| C.生成的氢气在标准状况下的体积为11.2 L |
| D.氢氧化钠溶液的物质的量浓度为5 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Al和Fe | B. Mg和Al | C.Fe和Cu | D.Na和Mg |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
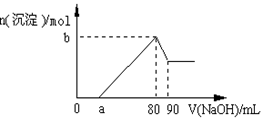
| A.盐酸的体积为80ml | B.a的取值范围为0<a<50 |
| C.n(Mg2+)<0.025mol | D.当a值为30时,b值为0.01 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温常压下,11.2 L氧气所含的O原子数为NA |
| B.1mol/L的CaCl2溶液中含有的Cl-为2NA |
| C.2.4g镁变成Mg2+时失去的电子数目为0.2NA |
| D.标准状况下,2g氢气所含原子数目为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.300ml 1mol·L-1氯化钠溶液 | B.150ml 2mol·L-1 氯化铵溶液 |
| C.75ml 3mol·L-1氯化钙溶液 | D.120ml 1.5mol·L-1氯化镁溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1L溶液中含有Na+、SO42-总数为0.3NA |
| B.1L溶液中含有Na+数目是0.15NA |
| C.1 L溶液中Na+的浓度是0.3 mol / L |
| D.2 L溶液中含有SO42—的浓度是0.3mol / L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com