
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法正确的是
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气
C.电池反应的化学方程式为CH3CH2OH+O2=CH3COOH+H2O
D.正极上发生的反应为O2+4e-+2H2O=4OH-
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源:2014高考名师推荐化学实验药品保存、基本操作、检验(解析版) 题型:填空题
已知A、B、C、D、E、F六种短周期元素中,A、B、C、D是组成蛋白质的基本元素;A与B的原子序数之和等于C原子核内的质子数;A与E、D与F分别位于同一主族,且F原子核内的质子数是D原子核外电子数的2倍。据此,请回答:
(1)F在周期表中的位置是 。
(2)由A、C、D、F按8:2:4:1原子个数比组成的化合物甲中含有的化学键类型为 ;甲溶液中各离子浓度由大到小的顺序为 (用离子浓度符号表示)。
(3)化合物乙由A、C组成且相对分子质量为32;化合物丙由A、D组成且分子内电子总数与乙分子内电子总数相等;乙与丙的反应可用于火箭发射(反应产物不污染大气),则该反应的化学方程式为 。
(4)由A、D、E、F组成的化合物丁能与硫酸反应并放出刺激性气味的气体,则丁的化学式为 ;实验测得丁溶液显弱酸性,由此你能得出的结论是 。
(5)由B、A按1:4原子个数比组成的化合物戊与D的常见气态单质及NaOH溶液构成原电池(如图),试分析:
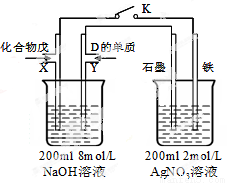
①闭合K,写出左池X电极的反应式 ;
②闭合K,当X电极消耗1.6g化合物戊时(假设过程中无任何损失),则右池两极共放出气体在标准状况下的体积为 升。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学基本营养物质(解析版) 题型:选择题
根据转化关系判断下列说法正确的是
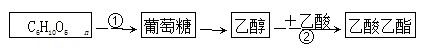
A.(C6H10O5)n可以是淀粉或纤维素,二者均属于多糖,互为同分异构体
B.可以利用银镜反应证明反应①的最终产物为葡萄糖
C.酸性高锰酸钾可将乙醇氧化为乙酸,将烧黑的铜丝趁热插入乙醇中也可得到乙酸
D.在反应②得到的混合物中倒入饱和氢氧化钠溶液并分液可得到纯净的乙酸乙酯
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学可充电池的反应规律(解析版) 题型:选择题
固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体。这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体。目前固体电解质在制造全固态电池及其他传感器、探测器等方面的应用日益广泛。如RbAg4I5晶体,其中迁移的物种全是Ag+,室温导电率达0.27 Ω-1·cm-1。利用RbAg4I5晶体,可以制成电化学气敏传感器。下图是一种测定O2含量的气体传感器示意图,被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量。在气体传感器工作过程中,下列变化肯定没有发生的是
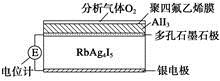
A.I2+2Rb++2e-=2RbIB.I2+2Ag++2e-=2AgI
C.Ag-e-=Ag+D.4AlI3+3O2=2Al2O3+6I2
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学可充电池的反应规律(解析版) 题型:选择题
镁及其化合物一般无毒(或低毒)、无污染,且镁电池放电时电压高而平稳。其中一种镁电池的反应为xMg+Mo3S4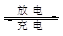 MgxMo3S4。下列说法错误的是
MgxMo3S4。下列说法错误的是
A.放电时Mg2+向正极迁移
B.放电时正极反应为Mo3S4+2xe-=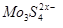
C.充电时Mo3S4发生氧化反应
D.充电时阴极反应为Mg2++2e-=Mg
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学原电池的工作原理、电极反应式的书写(解析版) 题型:选择题
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示,下列说法正确的是
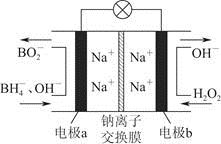
A.电池放电时,Na+从b极区移向a极区
B.电极a采用MnO2,放电时它被还原
C.该电池负极的电极反应式为BH+8OH--8e-=BO+6H2O
D.放电时,a极区溶液的pH升高,b极区溶液pH降低
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学原电池四种型与金属腐蚀、保护(解析版) 题型:选择题
将两个铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即可产生电流。下列叙述正确的是
①通入CH4的电极为正极 ②正极的电极反应式为O2+2H2O+4e-=4OH- ③通入CH4的电极反应式为CH4+2O2+4e-=CO2+2H2O ④负极的电极反应式为CH4+10OH--8e-=CO32-+7H2O ⑤放电时溶液中的阳离子向负极移动 ⑥放电时溶液中的阴离子向负极移动
A.①③⑤ B.②④⑥C.④⑤⑥ D.①②③
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学化学用语与分类(解析版) 题型:选择题
下列各项说法正确的是
①氢氧化铁胶体中,H+、K+、S2-、Br-能大量共存
②向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
③沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
④明矾能水解生成Al(OH)3胶体,可用作净水剂
⑤向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体
A.②④ B.②③⑤ C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学化学平衡图像(解析版) 题型:选择题
温度为T时,向2 L恒容密闭容器中充入1 mol PCl5,发生PCl5(g)  PCl3(g) + Cl2(g)反应。反应过程中c(Cl2) 随时间变化的曲线如下图所示,下列说法不正确的是
PCl3(g) + Cl2(g)反应。反应过程中c(Cl2) 随时间变化的曲线如下图所示,下列说法不正确的是
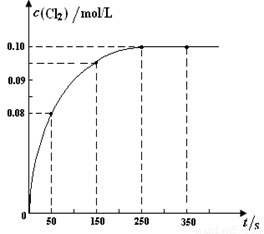
A.反应在0 ~50 s 的平均速率v(Cl2) =1.6×10-3mol/(L·s)
B.该温度下,反应的平衡常数K = 0.025
C.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol/L,则该反应的ΔH <0
D.反应达平衡后,再向容器中充入 1 mol PCl5,该温度下再达到平衡时,0.1 mol/L<c(Cl2)<0.2 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com