
| A. | “可燃冰”是将水变为油的新型燃料 | |
| B. | 氢气是具有热值高、无污染等优点的燃料 | |
| C. | 天然气、海洋能、太阳能、生物质能、风能、氢能 都属于新能源 | |
| D. | 电能是一次能源 |
分析 A.可燃冰”外观像冰,其化学组成是CH4•nH2O;
B.氢气的热值高,且燃烧产物是水;
C.天然气等是化石燃料,不是新能源;
D.自然界中以现成形式提供的能源称为一次能源,需要依靠他能源的能量间接制取的能源称为二次能源.
解答 解:A.可燃冰”外观像冰,其化学组成是CH4•nH2O,水的化学式为H2O,根据元素守恒知,水不能变为油,故A错误;
B.氢能源具有来源广、热值高,且燃烧后生成水对环境无污染,故B正确;
C.海洋能、太阳能、生物质能、风能、氢能 都属于新能源,而天然气是化石能源,故C错误;
D.电能是通过物质燃烧放热转化成的,或是由风能、水能、核能等转化来的,属于二次能源,故D错误;
故选B.
点评 本题考查环境污染、能源分类及应用,题目难度不大,注意掌握常见能源类型,明确一次能源与二次能源、化石能源与新能源区别为解答关键,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验设计 | |
| A. | 除去NaHCO3固体中的Na2CO3 | 将固体加热至恒重 |
| B. | 制备无水AlCl3 | 蒸发Al与稀盐酸反应后的溶液 |
| C. | 重结晶提纯苯甲酸 | 将粗品水溶、过滤、蒸发、结晶 |
| D. | 鉴别NaBr和KI溶液 | 分别加新制氯水后,用CCl4萃取 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①、②为反应③提供原料气 | |
| B. | 反应③也是 CO2资源化利用的方法之一 | |
| C. | 反应CH3OH(g)═$\frac{1}{2}$CH3OCH3 (g)+$\frac{1}{2}$H2O(l)的△H=$\frac{d}{2}$kJ•mol-1 | |
| D. | 反应 2CO(g)+4H2 (g)═CH3OCH3 (g)+H2O(g)的△H=( 2b+2c+d ) kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
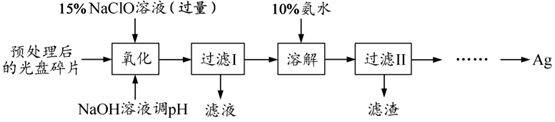
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.25g | B. | 1.32g | C. | 1.97g | D. | 2.44g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钾与硫酸的反应 | B. | 锌与盐酸反应放出氢气 | ||
| C. | CO2通过炽热的焦炭发生的反应 | D. | Ba(OH)2•8H2O与NH4Cl反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
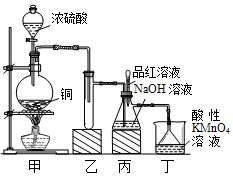 某化学兴趣小组设计实验,用浓硫酸与铜的反应制取SO2并进行相关实验探究,同时获得少量NaHSO3,实验装置如图所示:
某化学兴趣小组设计实验,用浓硫酸与铜的反应制取SO2并进行相关实验探究,同时获得少量NaHSO3,实验装置如图所示:| 实验操作 | 预期现象与结论 |
| 步骤1:取少量待测液放入试管中,滴加过量lmol/L氯化钡溶液.静置一段时间后,得到滤液A和固体B. | |
| 步骤2:往固体B中加入蒸馏水洗涤沉淀,静置后弃去上层清液,向固体滴入2滴(或少量)品红,再滴加盐酸. | 若品红褪色(或有气泡),则说明含有Na2SO3. |
| 步骤3:用试管取少量A,向其中加入过量的氢氧化钡溶液或先加入品红再加入盐酸. | 若若生成白色沉淀或品红褪色,则说明有NaHSO3生成; 否则不存在NaHSO3. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
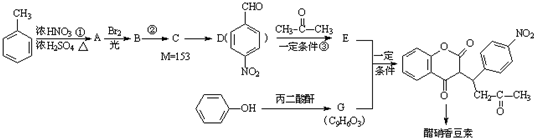

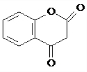 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com