
| A. | 改变温度,反应中转移电子的物质的量n的范围:3a mol≤n≤5a mol | |
| B. | 改变温度,产物中NaCl的最小理论产量为4a mol | |
| C. | 参加反应的氯气的物质的量3a mol | |
| D. | 某温度下,若反应后$\frac{c(C{l}^{-})}{c(Cl{O}_{3}^{-})}$=6,则溶液中$\frac{c(C{l}^{-})}{c(Cl{O}_{3}^{-})}$=6 |
分析 A.氧化产物只有KClO3时,转移电子最多,氧化产物只有KClO时,转移电子最少,根据电子转移守恒及钠离子守恒计算;
B.反应中转移电子最少时生成NaCl最少;
C.由Cl原子守恒可知,2n(Cl2)=n(NaCl)+n(NaClO)+n(NaClO3),由钠离子守恒可知n(NaCl)+n(NaClO)+n(NaClO3)=n(NaOH);
D.令n(ClO-)=1mol,反应后$\frac{c(C{l}^{-})}{c(Cl{O}_{3}^{-})}$=6,则n(Cl-)=6mol,根据电子转移守恒计算n(ClO3-),据此计算判断.
解答 解:A.氧化产物只有NaClO3时,转移电子最多,根据电子转移守恒n(NaCl)=5(NaClO3),由钠离子守恒:n(NaCl)+n(NaClO3)=n(NaOH),故n(NaClO3)=$\frac{1}{6}$n(NaOH)=$\frac{1}{6}$×6a mol,转移电子最大物质的量=a mol×5=5a mol,氧化产物只有NaClO时,转移电子最少,根据电子转移守恒n(NaCl)=n(NaClO),由钠离子守恒:n(NaCl)+n(NaClO)=n(NaOH),故n(NaClO)=$\frac{1}{2}$n(NaOH)=3a mol,转移电子最小物质的量=3a mol×1=3a mol,故反应中转移电子的物质的量n的范围:3amol≤n≤5amol,故A正确;
B.反应中还原产物只有NaCl,反应中转移电子最少时生成NaCl最少,根据电子转移守恒n(NaCl)=n(NaClO),由钠离子守恒:n(NaCl)+n(NaClO)=n(NaOH),故n(NaCl)=$\frac{1}{2}$n(NaOH)=3a mol,故B错误;
C.由Cl原子守恒可知,2n(Cl2)=n(NaCl)+n(NaClO)+n(NaClO3),由钠离子守恒可知n(NaCl)+n(NaClO)+n(NaClO3)=n(NaOH),故参加反应的氯气的物质的量=$\frac{1}{2}$n(NaOH)=3a mol,故C正确;
D.令n(ClO-)=1mol,反应后$\frac{c(C{l}^{-})}{c(Cl{O}_{3}^{-})}$=6,则n(Cl-)=6mol,电子转移守恒,5×n(ClO3-)+1×n(ClO-)=1×n(Cl-),即5×n(ClO3-)+1×1mol=1×6mol,解得n(ClO3-)=1mol,则溶液中$\frac{c(C{l}^{-})}{c(Cl{O}_{3}^{-})}$=6,故D正确;
故选B.
点评 本题考查了氧化还原反应计算,题目难度中等,注意电子转移守恒及极限法的应用,侧重于考查学生的分析能力和计算能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B的平均消耗速率为0.3mol(L•min) | |
| B. | C的平衡浓度为2mol/L | |
| C. | 平衡后,增大压强,平衡将向正方向移动 | |
| D. | 若单位时间内生成的B和C的物质的量之比为3:2,则体系处于平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图咖啡酸,存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好.
如图咖啡酸,存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好.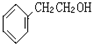 .
. 的一种同分异构体,A的苯环上有三个取代基,能发生银镜反应,苯环上的一氯代物有两种.写出A的一种结构简式:
的一种同分异构体,A的苯环上有三个取代基,能发生银镜反应,苯环上的一氯代物有两种.写出A的一种结构简式: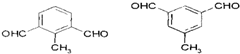 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 .下列关于有机物
.下列关于有机物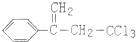 (除草剂,俗称稗草烯)的说法不正确的是( )
(除草剂,俗称稗草烯)的说法不正确的是( )| A. | 能使酸性高锰酸钾溶液褪色 | |
| B. | 在足量NaOH溶液中充分水解,可生成羧酸钠 | |
| C. | 可用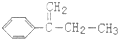 与Cl2在光照条件下通过取代反应获得较纯的该物质 与Cl2在光照条件下通过取代反应获得较纯的该物质 | |
| D. | 在一定条件下可发生聚合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
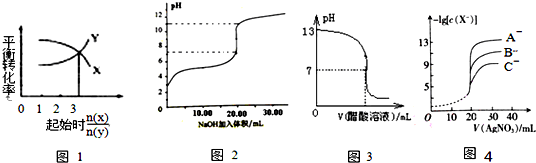
| A. | 一定条件下,X和Y反应生成Z,由图1推出该反应的方程式可表示为:X+3Y?Z | |
| B. | 图2表示NaOH溶液滴加到0.1 mol/L的一元酸溶液得到的滴定曲线(常温下),该实验最好选取酚酞作指示剂 | |
| C. | 常温下,向NaOH溶液中逐滴加入等浓度的醋酸溶液,所得滴定曲线如图3所示.当7<pH<13时,溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均可以与Ag+反应生成沉淀),由图4可确定首先沉淀的是A- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com