
对于反应2SO3(g)⇌2SO2)(g)+O2(g),若在一定温度下,将2mol SO3放入体积为2L的密闭容器中,当达到平衡状态时,测得O2的物质的量为0.6mol,求该反应的平衡常数.
考点:
化学平衡的计算.
专题:
化学平衡专题.
分析:
依据化学平衡三段式列式计算
2SO3(g)⇌2SO2(g)+O2(g)
起始量(mol) 2 0 0
平衡量(mol) 1.2 1.2 0.6
平衡量(mol) 0.8 1.2 0.6
据此计算平衡浓度=
平衡常数用生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积计算得到.
解答:
解:达到平衡状态时,测得O2的物质的量为0.6mol,则
2SO3(g)⇌2SO2(g)+O2(g)
起始量(mol) 2 0 0
平衡量(mol) 1.2 1.2 0.6
平衡量(mol) 0.8 1.2 0.6
平衡浓度c(SO3)=0.4mol/L,c(SO2)=0.6mol/L,c(O2)=0.3mol/L
反应的平衡常数K=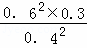 =0.675;
=0.675;
答:该反应的平衡常数0.675.
点评:
本题考查了化学平衡计算应用,平衡常数概念的计算应用掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:
取pH均等于2的盐酸和醋酸各100mL分别稀释2倍后,再分别加入过量的锌粉,在相同条件下充分反应,有关叙述正确的是( )
|
| A. | 盐酸与锌反应放出氢气多 |
|
| B. | 盐酸和醋酸分别与锌反应放出氢气一样多 |
|
| C. | 醋酸与锌反应速率较大 |
|
| D. | 盐酸和醋酸与锌反应的速率一样大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 书写热化学方程式时,只要在化学方程式的右端写上热量的符号和数值即可 |
|
| B. | 凡是在加热或点燃条件下进行的反应都是吸热反应 |
|
| C. | 表明反应所放出或吸收热量的化学方程式叫做热化学方程式 |
|
| D. | 氢气在氧气中燃烧的热化学方程式是:2H2(g)+O2(g)═2H2O(l);△H=﹣483.6 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
有相同pH的三种酸HX、HY、HZ的溶液,稀释相同倍数后,pH的变化值依次增大,则HX、HY、HZ的酸性由强到弱的顺序是( )
|
| A. | HX、HY、HZ | B. | HZ、HY、HX | C. | HX、HZ、HY | D. | HY、HZ、HX |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于下列反应:2SO2+O2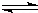 2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为 ,用O2浓度变化来表示的反应速率为 .如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L•min),那么2min时SO2的浓度为 .
2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为 ,用O2浓度变化来表示的反应速率为 .如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L•min),那么2min时SO2的浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在生产和日常生活中有着重要的应用。下列说法不正确的是
A.铁管道与直流电源负极相连,防止铁管道腐蚀
B.小苏打、氢氧化铝可用于治疗胃酸过多
C.工业生产中,常将氯气通入澄清石灰水中,制取漂白粉
B.除去氯化钙溶液中少量盐酸,加入足量碳酸钙粉末,充分搅拌再过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下钛的化学活性很小,在较高温度下可与多种物质反应。
(1)工业上由金红石(含TiO2大于96%)为原料生产钛的流程如下:
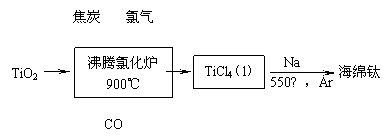

① 沸腾氯化炉中发生的主要反应为: 。
② 已知:Ti(s) +2Cl2(g)=TiCl4(l) ΔH=a kJ·mol-1;
2Na(s) +Cl2(g)=2NaCl(s) ΔH=b kJ·mol-1;
Na(s)=Na(l) ΔH=c kJ·mol-1;
则:TiCl4(l) +4Na(l)=Ti(s) +4NaCl(s) ΔH= kJ·mol-1。
(2)TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氯化钙,原理如下图所示,二氧化钛电极连接电源 极,该极电极反应为:
。但此法会产生有毒气体,为减少对环境的污染,在电池中加入固体氧离子隔膜(氧离子能顺利通过),将两极产物隔开,再将石墨改为金属陶瓷电极,并通入一种无毒的还原性气体,该气体是 。


(3)海绵钛可用碘提纯,原理为: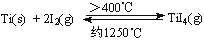 ,下列说法正确的是 。
,下列说法正确的是 。
A.该反应正反应的ΔH>0
B.在不同温度区域,TiI4的量保持不变
C.在提纯过程中,I2 的作用是将粗钛从低温区转移到高温区
D.在提纯过程中,I2 可循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分类标准和分类结果不科学的是()
选项 分类目标 分类标准 分类结果
A 化学反应 有无离子参加或生成 离子反应和非离子反应
B 有无单质参加或生成 氧化还原反应和非氧化还原反应
C 化学物质 分散质粒子大小 胶体、溶液和浊液
D 化合物在水溶液或熔融状态下能否导电 电解质和非电解质
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com