
(8分)甲醇是一种优质燃料,可制作燃料电池。
(1)工业上可用下列两种反应制备甲醇:
①CO(g) + 2H2(g)  CH3OH(g) ΔH1 ②CO2(g)+3H2(g)
CH3OH(g) ΔH1 ②CO2(g)+3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
已知:③2H2(g)+ O2(g) = 2H2O(g) ΔH3 。则2CO(g)+O2(g)=2CO2(g) 的反应热
ΔH=______(用ΔH1、ΔH2、ΔH3表示)。
(2)生产甲醇的原料CO和H2来源于:CH4(g) + H2O(g)  CO(g) + 3H2(g) ΔH4。
CO(g) + 3H2(g) ΔH4。
一定条件下CH4的平衡转化率与温度、压强的关系如图a。则ΔH4______0,P1_________P2
(填“<”、“>”或“=”)
某实验小组设计如图b所示的甲醇燃料电池装置,工作一段时间后,溶液的PH (填增大、 减小、不变)。负极的电极反应式为_______ ____。

(4)黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需进一步采用电解法精制。粗铜电解得到精铜的的电解池中,阳极材料是 ;阴极材料是 ;阳极泥为: 
(1)2△H1-2△H2+△H3; (2)>;<;
(3)减小 CH3OH-6e-+8OH-=CO32-+6H2O(4)粗铜,精铜,Ag、Au
【解析】
试题分析:(1)①×2-②×2+③,整理可得2CO(g)+O2(g)=2CO2(g) ΔH=2△H1-2△H2+△H3;(20由于升高温度,CH4的平衡转化率增大。根据平衡移动原理:升高温度,平衡向吸热反应方向移动,所以正反应方向是吸热反应,ΔH4>0;增大压强,平衡逆向移动,CH4的平衡转化率降低。根据图示可知P1<P2(3)某实验小组设计如图b所示的甲醇燃料电池装置,工作原理是2CH3OH+3O2+4KOH=2K2CO3+6H2O,可见工作一段时间后,溶液的pH减小。负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O。(4)黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需进一步采用电解法精制。粗铜电解得到精铜的的电解池中,阳极材料是粗铜,阴极材料是精铜;在阳极上Cu及活动性比Cu强的金属Fe等失去电子,变为金属阳离子进入溶液,而活动性比Cu弱的金属Ag、Au等就沉淀在阳极底层,俗称阳极泥,所以阳极泥为Ag、Au。
考点:考查盖斯定律的应用、温度、压强对物质转化率的影响、燃料电池的各种原理及电镀的知识。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源:2014-2015学年湖北咸宁鄂南高级中学高二起点考试化学(A类)试卷(解析版) 题型:填空题
(10分)已知H2A在水中存在以下平衡:H2A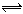 H++HA-,HA-
H++HA-,HA-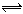 H++A2-。回答以下问题:
H++A2-。回答以下问题:
(1)NaHA溶液________(填“显酸性”、“显碱性”、“显中性”或“酸碱性无法确定” ,下同),某二元酸H2B电离方程式是:H2B H++HB-,HB- B2-+H+, NaHB溶液________。
B2-+H+, NaHB溶液________。
(2)某温度下,向0.1 mol/L的NaHA溶液中滴入0.1 mol/LKOH溶液至中性,此时溶液中以下关系一定正确的是________(填字母)。
A.c(H+)·c(OH-)=1×10-14 mol2/L2 B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+) D.c(Na+)+c(K+)=0.05 mol/L
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:
CaA(s) 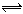 Ca2+(aq)+A2-(aq) ΔH>0。
Ca2+(aq)+A2-(aq) ΔH>0。
①温度升高时,Ksp________(填“增大”、“减小”或“不变”,下同)。
②滴加少量浓盐酸,c(Ca2+)________,原因是
__________________________________________(用文字和离子方程式说明)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏江阴高一上暑期学习反馈(开学检测)化学试卷(解析版) 题型:选择题
根据某种共性,可将SO3、CO2归为同类氧化物。下列物质中也属于这类氧化物的是
A.CaCO3 B.SO2 C.KMnO4 D.Na2O
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
将0.195g锌粉加入到20.0mL的0.100 mol·L-1MO2+溶液中,恰好完全反应,则还原产物可能是( )
A. M B. M2+ C.M3+ D. MO2+
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
现有四种元素的基态原子的电子排布式如下:① [Ne]3s23p4; ②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是( )
A.最高正化合价:③>②>① B.第一电离能:③>②>①
C.电负性:③>②>① D.原子半径:③>②>①
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:填空题
(5分)在固定容积的密闭容器中,有可逆反应nA(g)+mB(g) pC(g)处于平衡状态(已知n+m>p,△H>0)。升高温度时c(B)/c(C)的比值 ,混合气体的密度 ;降温时,混合气体的平均相对分子质量 ;加入催化剂,气体的总物质的量 ;充入C,则A、B的物质的量 。(填增大、减小、不变、不确定)
pC(g)处于平衡状态(已知n+m>p,△H>0)。升高温度时c(B)/c(C)的比值 ,混合气体的密度 ;降温时,混合气体的平均相对分子质量 ;加入催化剂,气体的总物质的量 ;充入C,则A、B的物质的量 。(填增大、减小、不变、不确定)
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
 从H+、K+、Cu2+、Cl-、SO
从H+、K+、Cu2+、Cl-、SO 中选取适当的离子组成符合下列情况的电解质。惰性电解,电 解质的物质的量减少,水的物质的量也减少,pH下降,则电解质的化学式为( )
中选取适当的离子组成符合下列情况的电解质。惰性电解,电 解质的物质的量减少,水的物质的量也减少,pH下降,则电解质的化学式为( )
A、HCl B、K2SO4 C、CuSO4 D、KCl
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:填空题
(8分)实验室用固体烧碱配制0.1 mol /L的NaOH溶液500 mL,回答下列问题:
(1)计算需要NaOH固体的质量 g。
(2)有以下仪器和用品:①烧杯②药匙③250 mL容量瓶④500 mL容量瓶⑤玻璃棒⑥托盘天平。配制时,必须使用的仪器或用品有 (填序号),还缺少的仪器是 。
(3)使用容量瓶前必须进行的第一步操作是 。
(4)配制时,一般分为以下几个步骤:① 称量② 计算③ 溶解④ 摇匀⑤ 转移⑥ 洗涤⑦ 定容,
其正确的操作顺序为 。
(5)配制过程中,下列操作会引起结果偏高的是 (填序号)。
① 未洗涤烧杯、玻璃棒 ② NaOH溶液未冷却至室温就转移到容量瓶并定容
③ 容量瓶不干燥,含有少量蒸馏水 ④ 称量NaOH的时间太长 ⑤ 定容时俯视刻度
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
CuSO4是一种重要的化工原料,有关制备途径及性质如下图所示。下列说法错误的是( )

A.途径①所用混酸中H2SO4与HNO3的最佳物质的量之比为3:2
B.与途径①、③相比,途径②更好地体现了绿色化学思想
C.生成等量的硫酸铜,三个途径中参加反应的硫酸的物质的量①=②<③
D.利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com