
A、 |
B、 |
C、 |
D、 |
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案科目:高中化学 来源: 题型:
| A、a=b | ||
| B、混合溶液的pH=7 | ||
C、混合溶液中,c(H+)=
| ||
| D、向反应后的混合液中滴加石蕊试液后呈紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、电池放电时,负极失去电子,质量减轻 |
| B、电池放电时,电解质溶液中的H+向负极移动 |
| C、电池充电时,电池正极应和外接电源的正极相连接 |
| D、电池充电时,阴极反应为:Pb-2e-+SO42-=PbSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A、已知醋酸铵溶液呈中性,在①、②两中分别加入适量的氯化铵晶体或醋酸铵晶体后,两溶液的pH均减小 |
| B、四种溶液分别加水稀释10倍,四种溶液的pH①>②>④>③ |
| C、①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、VaL④溶液与VbL②溶液混合后,若混合后溶液pH=4,则Va:Vb=11:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:

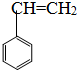 ;②CH3-CH=CH-CH3; ③CH2=CH-CH=CH2;④CH≡C-CH3;⑤
;②CH3-CH=CH-CH3; ③CH2=CH-CH=CH2;④CH≡C-CH3;⑤
| A、①② | B、④⑤ | C、③⑤ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| W | X | Y |
| Z |
| 编号 | 推测性质 | 化学方程式 |
| 示例 | 氧化性 | H2ZO3+4HI=Z↓+2I2+3H2O |
| ① | ||
| ② | H2ZO3+Br2+H2O=H2ZO4+2HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com