
| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| B. | 等物质的量的MgCl2、Ba(OH)2 和 HC1溶液混合:Mg2++2OH-=Mg(OH)2↓ | |
| C. | 酸性介质中KMnO4氧化 H2O2:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O | |
| D. | 二氧化硫通入次氯酸钠溶液:SO2+ClO-+2OH-=SO42-+Cl-+H2O |
分析 A.二者反应生成硫酸钡和水;
B.先发生中和反应,氢氧根离子有一半没有发生中和反应,剩余的氢氧根离子和镁离子反应生成氢氧化镁沉淀;
B.二者发生氧化还原反应生成锰离子、氧气和水;
D.二者发生氧化还原反应生成硫酸根离子和氯离子.
解答 解:A.二者反应生成硫酸钡和水,离子方程式为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故A正确;
B.先发生中和反应,氢氧根离子有一半没有发生中和反应,剩余的氢氧根离子和镁离子反应生成氢氧化镁沉淀,离子方程式为Mg2++2H++4OH-=Mg(OH)2↓+2H2O,故B错误;
B.二者发生氧化还原反应生成锰离子、氧气和水,离子方程式为2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O,故C正确;
D.二者发生氧化还原反应生成硫酸根离子和氯离子,离子方程式为SO2+ClO-+2OH-=SO42-+Cl-+H2O,故D正确;
故选B.
点评 本题考查离子方程式正误判断,为高频考点,侧重考查学生分析判断及应用能力,明确离子方程式书写特点及物质性质是解本题关键,易错选项是BD,题目难度中等.


科目:高中化学 来源: 题型:解答题
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
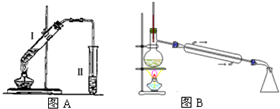
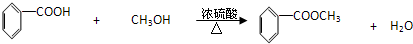 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
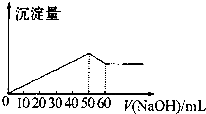
| A. | 6:1 | B. | 3:1 | C. | 3:4 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 移去部分SO3 | B. | 增大容器容积 | C. | 降低体系温度 | D. | 通入大量O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为除去FeSO4溶液中的Fe2(SO4)3,可加入铁粉,再过滤 | |
| B. | SO2使溴水褪色,不能说明SO2具有漂白性 | |
| C. | HCl、NO2溶于水都有化学键断裂,但不全属于化学变化 | |
| D. | 为除去CO2中少量的SO2,可使其通过饱和Na2CO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com