
分析 ①普通玻璃成分是:二氧化硅,硅酸钠和硅酸钙;石英和碳酸钠高温下反应生成Na2SiO3和CO2;
②钢铁是金属铁和碳的合金;根据铁器件的烤蓝原理解答;形成原电池后,会加快负极金属的腐蚀速率,正极金属始终被保护.
③硫化前后,橡胶橡胶分子发生了变化生成了别的大分子有机物,结构由链状变成了网状.
解答 解:①工业制玻璃主要原料有石英、纯碱和石灰石,高温下,碳酸钙和二氧化硅反应生成硅酸钙和二氧化碳,高温下,碳酸钠和二氧化硅反应生成硅酸钠和二氧化碳,所以普通玻璃主要成分是Na2SiO3、CaSiO3和SiO2;石英和碳酸钠高温下反应生成Na2SiO3和CO2:SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑.
故答案为:SiO2;SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑.
②钢铁是铁和碳的合金;增强铁器件的抗腐蚀能力,烤蓝是利用碱性氧化性溶液的氧化作用,在钢铁表面形成一层深蓝色的Fe3O4薄膜,保护内部金属免受腐蚀;当镀锌的铁的镀层被损坏后,金属铁、锌以及电解质形成原电池,金属铁为正极,被被保护起来,这时被腐蚀速度比普通铁慢.故答案为:碳;Fe3O4;慢.
③硫化前后,橡胶橡胶分子发生了变化生成了别的大分子有机物,结构由链状变成了网状,故答案为:硫化.
点评 本题考查内容较多,是一道综合题,侧重考查了玻璃的成分、铁的冶炼原理、金属的吸氧腐蚀以及金属的防护知识,注意知识的积累和教材知识的灵活应用是解题的关键,题目难度中等.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:解答题
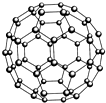 (1)铬的外围电子排布式是3d54s1,与铬同周期,最外层有3个未成对电子数的元素名称是砷,该元素对应的最低价氢化物分子的中心原子采取
(1)铬的外围电子排布式是3d54s1,与铬同周期,最外层有3个未成对电子数的元素名称是砷,该元素对应的最低价氢化物分子的中心原子采取| 元 素 | X | Y | Z |
| 电 负 性 | 1.5 | 1.2 | 1.8 |
| 第一电离能/kJ•mol-1 | 578 | 738 | 787 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
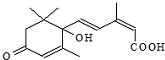
| A. | 分子式C15H21O4 | |
| B. | 既能发生加聚反应,又能发生缩聚反应 | |
| C. | 分子中有三种官能团 | |
| D. | 既能使氯化铁溶液发生显色反应,又能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸电离出的H+离子,能被Zn、Fe等金属还原成H2 | |
| B. | 浓HNO3与浓HCl按3:1的体积比所得的混合物叫王水 | |
| C. | 硝酸与金属反应时,主要是+5价的氮元素得电子 | |
| D. | 常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,B2H6和C2H4的混合气体22.4L,所含的电子数约为16NA | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 标准状况下,1L庚烷所含有的分子数为$\frac{{N}_{A}}{22.4}$ | |
| D. | 26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ②③⑧ | C. | ③④⑤⑦⑧ | D. | ②⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
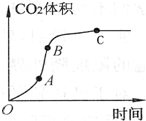 某学生用优质大理石与稀盐酸反应制取CO2,(不考虑反应过程中溶液体积
某学生用优质大理石与稀盐酸反应制取CO2,(不考虑反应过程中溶液体积| A. | AB段反应速率最快的原因可能是反应放热,体系温度升高 | |
| B. | BC段反应速率变慢的原因可能是盐酸浓度降低 | |
| C. | 该反应速率也可以用CaCl2的浓度变化与时间关系来表示 | |
| D. | C点后CO2体积不变的原因一定是盐酸消耗完 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2可以使Br2水褪色,是因为SO2具有漂白性 | |
| B. | Na的金属活性比Mg强,故可用Na与MgCl2溶液反应制Mg | |
| C. | Fe在Cl2中燃烧生成FeCl3,故Fe与I2反应生成FeI3 | |
| D. | 可以用铝制的容器储存和运输浓硝酸是因为常温下铝遇到浓硝酸钝化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com