
| A£® | ĻąĶ¬ÖŹĮæµÄCŗĶDµ„ÖŹ·ÖeÓė×ćĮæĻ”ŃĪĖį·“Ó¦Ź±£¬ŗóÕßÉś³ÉµÄĒāĘų¶ą | |
| B£® | CÓėDµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļµÄ¼īŠŌĻą±Č£¬ŗóÕßøüĒæ | |
| C£® | ²»ÓƵē½āĀČ»ÆĪļµÄ·½·ØÖʱøµ„ÖŹDŹĒÓÉÓŚĘäĀČ»ÆĪļµÄČŪµćøß | |
| D£® | ¼ņµ„Ąė×Ó°ė¾¶£ŗB£¼C |
·ÖĪö ¶ĢÖÜĘŚA”¢B”¢C”¢D”¢EĪåÖÖÖ÷×åŌŖĖŲ£¬Ō×ÓŠņŹżŅĄ“ĪŌö“ó£¬CŹĒĶ¬ÖÜĘŚÖŠŌ×Ó°ė¾¶×ī“óµÄŌŖĖŲ£¬CĪŖNa£»¹¤ŅµÉĻŅ»°ćĶعżµē½āŃõ»ÆĪļµÄ·½·Ø»ńµĆDµÄµ„ÖŹ£¬DĪŖAl£»Eµ„ÖŹŹĒÖʱøĢ«ŃōÄܵē³ŲµÄÖŲŅŖ²ÄĮĻ£¬EĪŖSi£¬B”¢C”¢E×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ11£¬ŌņBµÄ×īĶā²ćµē×ÓŹżĪŖ11-4-1=6£¬ŌņBĪŖO£¬AŌ×Ó×īĶā²ćµē×ÓŹżŹĒ“ĪĶā²ćµē×ÓŹżµÄ2±¶£¬AĪŖC£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗÓÉÉĻŹö·ÖĪöæÉÖŖ£¬AĪŖC£¬BĪŖO£¬CĪŖNa£¬DĪŖAl£¬EĪŖSi£¬
A£®ÉčÖŹĮæ¾łĪŖm£¬Óɵē×ÓŹŲŗćæÉÖŖ£¬$\frac{m}{23}$£¼$\frac{m}{27}$”Į£Ø3-0£©£¬ŌņĻąĶ¬ÖŹĮæµÄCŗĶDµ„ÖŹ·ÖeÓė×ćĮæĻ”ŃĪĖį·“Ó¦Ź±£¬ŗóÕßÉś³ÉµÄĒāĘų¶ą£¬¹ŹAÕżČ·£»
B£®½šŹōŠŌNa£¾Al£¬CÓėDµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļµÄ¼īŠŌĻą±Č£¬Ē°ÕßøüĒ棬¹ŹB“ķĪó£»
C£®DµÄĀČ»ÆĪļĪŖ¹²¼Ū»ÆŗĻĪļ£¬²»µ¼µē£¬¹ŹC“ķĪó£»
D£®¾ßÓŠĻąĶ¬µē×ÓÅŲ¼µÄĄė×ÓÖŠŌ×ÓŠņŹż“óµÄĄė×Ó°ė¾¶Š”£¬Ōņ¼ņµ„Ąė×Ó°ė¾¶£ŗB£¾C£¬¹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éŌ×Ó½į¹¹ÓėŌŖĖŲÖÜĘŚĀÉ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŌŖĖŲµÄŠŌÖŹ”¢ŌŖĖŲ»ÆŗĻĪļ”¢Ō×Ó½į¹¹Ą“ĶʶĻŌŖĖŲĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅā¹ęĀÉŠŌÖŖŹ¶µÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
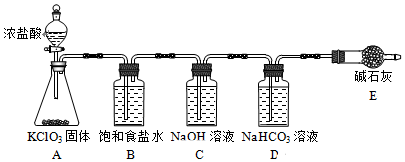
| ŹµŃé²½Öč | ŹµŃéĻÖĻó | ||
| BĘæ | CĘæ | DĘæ | |
| ŹµŃé1£ŗȔѳ£¬µĪ¼Ó×ĻÉ«ŹÆČļČÜŅŗ | ±äŗģ£¬²»ĶŹÉ« | ±äĄ¶£¬²»ĶŹÉ« | Į¢¼“ĶŹÉ« |
| ŹµŃé2£ŗȔѳ£¬²ā¶ØČÜŅŗµÄpH | 3 | 12 | 7 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
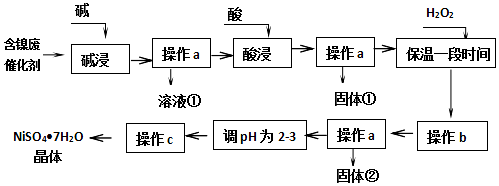
| ³ĮµķĪļ | æŖŹ¼³Įµķ | ĶźČ«³Įµķ |
| Al£ØOH£©3 | 3.8 | 5.2 |
| Fe£ØOH£©3 | 2.7 | 3.2 |
| Fe£ØOH£©2 | 7.6 | 9.7 |
| Ni£ØOH£©2 | 7.1 | 9.2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
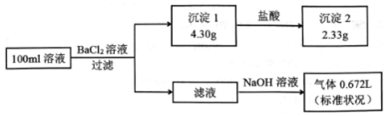
| A£® | ŌČÜŅŗŅ»¶Ø“ęŌŚCO32-ŗĶSO42-£¬Ņ»¶Ø²»“ęŌŚFe3+ | |
| B£® | ŹĒ·ń“ęŌŚNa+Ö»ÓŠĶعżŃęÉ«·“Ó¦²ÅÄÜČ·¶Ø | |
| C£® | ŌČÜŅŗŅ»¶Ø“ęŌŚNa+£¬æÉÄÜ“ęŌŚCl- | |
| D£® | ČōŌČÜŅŗÖŠ²»“ęŌŚCl-£¬Ōņc £ØNa+£©=0£®lmol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ca2+£¬Na+£¬NO3-£¬Cl- | B£® | K+£¬Ba2+£¬Cl-£¬NO3- | ||
| C£® | Na+£¬HCO3-£¬CO32-£¬K+ | D£® | Na+£¬Cl-£¬K+£¬MnO4- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1£ŗ3 | B£® | 3£ŗ1 | C£® | 3£ŗ2 | D£® | 1£ŗ2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ąė×Ó×é | ¼ÓČėŹŌ¼Į | ¼ÓČėŹŌ¼Įŗó·¢Éś·“Ó¦ | |
| A | K+”¢Fe2+”¢I- | ÉŁĮæµÄĖįŠŌKMnO4ČÜŅŗ | 5Fe2++MnO4-+8H+ØT5Fe3++Mn2++4H2O |
| B | Fe3+”¢I-”¢SO42- | NaOHČÜŅŗ | Fe3++3OH-ØTFe£ØOH£©3”ż |
| C | Ba2+”¢HCO3-”¢Cl- | NaOHČÜŅŗ | HCO3-+OH-ØTCO32-+H2O |
| D | Al3+”¢Cl-”¢NO3- | ¹żĮæÅØ°±Ė® | Al3++3NH3•H2OØTAl£ØOH£©3”ż+3NH4+ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1£ŗ1 | B£® | 2£ŗ1 | C£® | 1£ŗ2 | D£® | 2£ŗ3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com