
【题目】下列各组物质中,全部是强电解质的一组是
A.酒精、醋酸B.氯化钠、盐酸
C.碳酸钙、碳酸钡D.硝酸钾、碳酸
科目:高中化学 来源: 题型:
【题目】工业上制备纯净的氯化锌时,将含杂质的氯化锌溶于过量的盐酸中,为了除去杂质需要调节溶液的pH到4,应加入的试剂是
A.氢氧化钠B.氨水C.氧化锌D.氯化锌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 反应中,被氧化的物质是氧化剂
B. 氧化还原反应的本质是电子的转移
C. 某物质的元素在反应中失去电子,则此物质是氧化剂
D. 离子反应可能是复分解反应,但离子反应一定不是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜有两种天然同位素63Cu和65Cu,铜的相对原子质量为63.5,则63Cu原子所占的原子个数百分比是
A.20%B.25%C.30%D.75%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸甲酯是一种重要的工业原料,某研究性学习小组的同学拟用如图装置制取高纯度的苯甲酸甲酯. 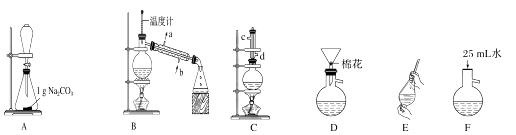
熔点/℃ | 沸点/℃ | 密度/gcm﹣3 | 水溶性 | |
苯甲酸 | 122.4 | 249 | 1.27 | 微溶 |
甲醇 | ﹣97 | 64.3 | 0.79 | 互溶 |
苯甲酸甲酯 | ﹣12.3 | 199.6 | 1.09 | 不溶 |
有关数据如表所示,请回答下列问题:
(1)在烧瓶中混合有机物及浓硫酸的方法是 , 装置C如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是 .
(2)B装置的冷凝管的主要作用是 , 可否换为球形冷凝管(填“可”或“否”).
(3)制备和提纯苯甲酸甲酯的操作先后顺序为(填装置字母代号).
(4)A中Na2CO3的作用是;D装置的作用是
(5)在洗涤、分液操作中,应充分振荡,然后静置,待分层后(填标号). a.直接将苯甲酸甲酯从分液漏斗的上口倒出
b.直接将苯甲酸甲酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将苯甲酸甲酯从下口放出
d.先将水层从分液漏斗的下口放出,再将苯甲酸甲酯从上口倒出.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、 ![]() (PAN)等二次污染物.
(PAN)等二次污染物.
①1mol PAN中含有的σ键数目为 . PAN中四种元素的第一电离能由大到小的顺序为 .
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4 , 该配合物中中心离子的配位数为 , 中心离子的核外电子排布式为 .
③相同压强下,HCOOH的沸点比CH3OCH3(填“高”或“低”),其原因是 .
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等.
①(NH4)2SO4晶体中各种微粒间的作用力不涉及(填序号).
a.离子键 b.共价键 c.配位键 d.范德华力 e.氢键
②NH4NO3中阳离子的空间构型为 , 阴离子的中心原子轨道采用杂化.
(3)测定大气中PM2.5的浓度方法之一是β﹣射线吸收法,β﹣射线放射源可用85Kr.已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则 ![]() =(填数字).
=(填数字).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com