
用NA表示阿伏加德罗常数.下列叙述正确的是( )
|
| A. | 1mol乙烯分子中含有的共用电子对的数目为5NA |
|
| B. | 42g乙烯与丙烯的混合气体中含碳原子数为3NA |
|
| C. | 标准状况下,22.4L己烷中碳碳键数目为5NA |
|
| D. | 乙烯和乙醇的混合物共0.1mol,完全燃烧所消耗的氧气分子数一定为0.6 NA |
| 阿伏加德罗常数. | |
| 专题: | 阿伏加德罗常数和阿伏加德罗定律. |
| 分析: | A.乙烯分子中含有4个碳氢共用电子对和2个碳碳共用电子对,总共含有6个共用电子对; B.乙烯和丙烯的最简式为CH2,根据二者的最简式计算出混合物中含有的碳原子数目; C.标况下己烷不是气体,不能使用标况下的气体摩尔体积计算己烷的物质的量; D.0.1mol乙烯消耗0.3mol氧气,0.1mol乙醇消耗0.3mol氧气,所以0.1mol乙醇与乙烯的混合物完全燃烧消耗的氧气的物质的量为0.3mol. |
| 解答: | 解:A.1mol乙烯中含有4mol碳氢共用电子对、2mol碳碳共用电子对,总共含有6mol共用电子对,含有的共用电子对的数目为6NA,故A错误; B.42g乙烯和丙烯的混合物中含有3mol最简式为CH2,含有3mol碳原子,含碳原子数为3NA,故B正确; C.标况下己烷不是气体,不能使用标况下的气体摩尔体积计算22.4L己烷的物质的量,故C错误; D.0.1mol乙烯和0.1mol乙醇完全燃烧消耗的氧气都是0.3mol,则乙烯和乙醇的混合物共0.1mol,完全燃烧所消耗的氧气为0.3mol,所消耗的氧气分子数一定为0.3NA,故D错误; 故选B. |
| 点评: | 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项AD为易错点,注意合理分析题干信息,如乙烯中存在2个碳碳共用电子对. |


科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.浓硫酸滴在润湿的蓝色石蕊试纸上,试纸先变红,然后褪色,最后变黑,说明浓硫酸具有酸性、氧化性和吸水性
B.样品 无明显现象
无明显现象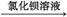 出现白色沉淀,说明样品中含S
出现白色沉淀,说明样品中含S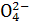
C.常温下浓硫酸能用铁制容器盛装,说明浓硫酸与Fe不反应
D.样品 得到使澄清石灰水变浑浊的气体,说明样品中含S
得到使澄清石灰水变浑浊的气体,说明样品中含S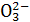 或HS
或HS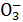
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,正确的是 ( )
A.原子半径:X>Y>Z>W B.金属性:X<Y,还原性:W 2- > Z-
C.原子最外层电子数:Y>X>Z>W D.原子序数:Y>X>Z>W
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室进行物质制备,下列从原料及试剂分别制取相应的最终产物的设计中,理论上正确、操作上可行、经济上合理的是( )
|
| A. | C |
|
| B. | Cu |
|
| C. | Fe |
|
| D. | CaO |
查看答案和解析>>
科目:高中化学 来源: 题型:
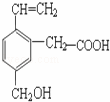
某有机物的结构为图,该有机物不可能具有的性质是( )
①可以燃烧氧化 ②能使酸性KMnO4溶液褪色 ③能跟NaOH溶液反应
④能发生分子内酯化反应 ⑤能发生加聚反应 ⑥它有手性碳原子
⑦能被催化氧化成醛.
|
| A. | ①④ | B. | ④⑥ | C. | ⑤⑦ | D. | 只有⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
有反应:4NH3+5O2→4NO+6H2O(g),下列有关该反应的速率关系正确的是( )
|
| A. | 4v(NH3)=5v(O2) | B. | 5v(O2)=4v(NO) | C. | 2v(NO)=3v(H2O) | D. | 5v(H2O)=6v(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应C(s)+H2O(g)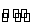 CO(g)+ H2(g)在一体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+ H2(g)在一体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.增加C的量
B.将容器体积缩小一倍
C.保持体积不变,充入N2使体系压强增大
D.保持压强不变,充入N2使体系体积增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com